Stop and think about your bones: what images come to mind? Misschien een schedel met grijnzende kaken, of de sterke witte ledematen die zich uitstrekken naar je vingers en tenen. Je zou zelfs kunnen denken aan het beenmerg in hen, het produceren van het bloed dat stroomt door uw aderen. Maar dit is niet het hele plaatje, want je skelet verbergt een geheim: het is vol vet, en niemand weet waarom.,
een onopgelost mysterie
Dit onopgeloste mysterie is verrassend. Wetenschappers merkten voor het eerst dat ons beenmerg vetopslagende cellen bevat, adipocyten genaamd, meer dan een eeuw geleden.1 het hebben van adipocyten in onze botten lijkt misschien ongebruikelijk, maar dat is het niet: bij zoogdieren ontwikkelt het vetweefsel van het beenmerg zich gestaag na de geboorte en accumuleert het zich snel tijdens de puberteit, zodat het tegen de tijd dat we de volwassenheid bereiken, tot 70% van het beenmergvolume kan uitmaken-dit vertegenwoordigt meer dan 8% van de totale vetmassa!,2
MAT is niet gelijkmatig verdeeld over het skelet, maar overheerst in de armen en benen. Deze perifere MAT ontwikkelt zich vroeg na de geboorte en is zelden uitgeput, en wordt daarom ‘constitutieve MAT’ (cMAT) genoemd.3 daarentegen bevatten meer centrale plaatsen, zoals de wervelkolom, het bekken en het borstbeen, evenals meer proximale gebieden van de lange beenderen, minder MAT en meer hematopoëtische rode merg (zie figuur)., Op deze plaatsen zijn de beenmergadipocyten meer diffuus en neigen zij om in reactie op milieu of pathologische factoren te verhogen of te verminderen; vandaar, is dit depot ‘gereguleerde MAT’ (rMAT) genoemd.3
andere eigenschappen van beenmergadipocyten variëren ook tussen deze skeletplaatsen, met mogelijke implicaties voor de impact van MAT op gezondheid en ziekte.2,3 de MAT neemt inderdaad verder toe naarmate de huid ouder wordt en onder uiteenlopende klinische omstandigheden, waaronder skeletaandoeningen, metabole en hematologische aandoeningen (figuur)., Daarom trekt MAT nu als potentiële speler veel belangstelling voor de ontwikkeling van talrijke ziekten. Nochtans, in tegenstelling tot witte en bruine vetweefsels (wat en vleermuis respectievelijk), is de studie van MAT vrij beperkt geweest. Bijgevolg blijven de fysiologische en pathologische functies van MAT slecht begrepen.4 dus, wat is de functie van MAT, en hoe kan het de menselijke gezondheid beïnvloeden?
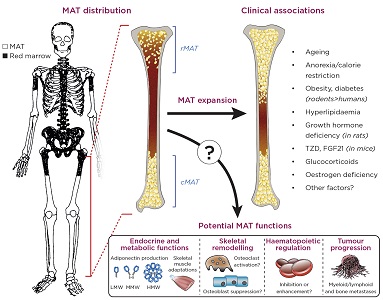
De anatomische distributie, klinische associaties en potentiële functies van beenmergvet Weefsel (MAT)., Het beeld van het skelet is gebaseerd op Kricun (1985).16 cMAT, constitutive MAT; rMAT, regulated MAT; TZD, thiazolidinediones; FGF21, fibroblast growth factor 21; LMW/MMW/HMW, low/medium/high molecular weight. Kricun ME 1985 rood-geel merg conversie: het effect op de locatie van enkele Solitaire botlaesies. Skeletale radiologie 14 (1), pp.10-19. ©International Skeletal Society 1985. Met toestemming van Springer.
slecht tot op het bot?,
verhoogde adipositeit van het beenmerg (BMA) wordt geassocieerd met een lagere botmineraaldichtheid en een verhoogde kwetsbaarheid van het skelet, bijvoorbeeld bij osteoporose, veroudering en oestrogeendeficiëntie.5 Dit heeft onderzoek gemotiveerd naar hoe MAT een impact heeft op de integriteit van het skelet.
Eén mogelijkheid is dat beenmergadipocyten dezelfde voorloper van skeletstamcellen delen als botvormende osteoblasten, in welk geval de accumulatie van de MAT ten koste van de ontwikkeling van osteoblast kan gaan.,6 echter, terwijl dit waar is tijdens de embryonale ontwikkeling, is het niet stevig gevestigd als deze gemeenschappelijke voorloper blijft tot volwassenheid om bij te dragen aan postnatale weefselonderhoud.
een andere mogelijkheid is dat beenmergadipocyten lokale factoren afscheiden die de botvorming direct beïnvloeden en/of de botresorptie stimuleren, waardoor het risico op fracturen toeneemt.7 intrigerend, kunnen dergelijke paracriene acties ook de groei van tumoren in het bot bevorderen, of primaire myeloïde/lymfoïde kankers, of metastasen van elders (figuur).,8,9
is de accumulatie van MAT daarom slecht voor de gezondheid van het bot? Helaas is het nog te vroeg om dat te zeggen. Hoewel een verhoogde MAT geassocieerd kan zijn met een verhoogd risico op fracturen, is een verhoogde MAT niet altijd geassocieerd met botverlies. De potentiële impact van MAT op de ontwikkeling van skelettumoren moet ook nog volledig worden begrepen. Gezien de volksgezondheidsuitdagingen die worden gesteld door osteoporose, skeletkanker en verouderingsgerelateerde ziekten, is het ophelderen van deze functies van MAT een belangrijk doel van lopend onderzoek.,
hematologie
de belangrijkste functie van beenmerg is in de bloedcelproductie, dus het is niet verwonderlijk dat veel van de vroegste studies van MAT werden uitgevoerd vanuit een hematologisch perspectief. Over het algemeen wordt een verlaagde BMA geassocieerd met een verhoogde hematopoëse 10,wat wijst op een onderdrukkend effect van MAT.
ter ondersteuning van deze mogelijkheid bleek uit een mijlpaal van 2009 dat accumulatie van blokkerende MAT het hematopoëtische herstel na beenmergtransplantatie verbetert.,Dit heeft belangrijke translationele implicaties: veel ontvangers van beenmergtransplantaties vertonen een slecht herstel op lange termijn, en daarom zou het onderdrukken van de adipogenese van het beenmerg een nieuwe therapeutische benadering kunnen zijn.
echter, niet alle gegevens ondersteunen een negatief effect op hematopoëse. Recent onderzoek suggereert inderdaad dat, in de context van beenmergtransplantaties, beenmergadipocyten een molecuul afscheiden dat stamcelfactor wordt genoemd, waardoor ze hematopoëse en de regeneratie van hematopoëtische stamcellen bevorderen.,12 wat de vermeende effecten van MAT op het bot betreft, blijkt de invloed ervan op de hematopoëse complexer te zijn dan aanvankelijk werd vermoed (figuur).
voorbij het bot: metabole en endocriene functies
hoewel de functies van MAT in het bot en het beenmerg nog niet definitief zijn vastgesteld, lijkt het duidelijk dat beenmergadipocyten de skelethomeostase en hematopoëse kunnen beïnvloeden door lokaal werkende factoren uit te scheiden. Maar scheidt MAT, net als WAT, ook endocriene producten af om systemische metabolische effecten uit te oefenen?
recente studies van onze laboratoria en anderen ondersteunen deze mogelijkheid., Talrijke rapporten tonen aan dat de beendermerg adipocytes leptin, het prototypical adipocyte-afgeleide hormoon produceren dat een belangrijke invloed over energiehomeostase, ontsteking en reproductieve functie heeft.7 We hebben ontdekt dat, net als in WAT,leptine expressie in MAT wordt onderdrukt als reactie op verminderde calorie-inname, 13 waaruit blijkt dat MAT en WAT gemeenschappelijke mechanismen delen om hun endocriene functies te reguleren.
of MAT bijdraagt aan circulerend leptine blijft onbekend, maar de functie ervan als bron van andere endocriene factoren wordt duidelijk., Een belangrijke nadruk van ons onderzoek is geweest op MAT als bron van adiponectin, het andere belangrijke hormoon geproduceerd door vetweefsel. Ondanks deze vetbron, wordt het doorgeven van adiponectin verminderd in zwaarlijvigheid en verhoogd in Staten van magerheid, zoals tijdens calorische beperking. Zelfs na 20 jaar van uitgebreid onderzoek naar adiponectine, was de basis voor deze zogenaamde ‘adiponectin paradox’ onvolledig begrepen gebleven; waarom zou een vet-afgeleid hormoon worden verhoogd wanneer wat ontbreekt?
Het was door deze lens dat we MAT in een nieuw licht begonnen te bekijken., In schril contrast met WAT, neemt de vorming van de MAT toe in uithongeringstoestanden, zoals tijdens calorische beperking in dieren en in menselijke patiënten met anorexia nervosa ‘ s.Zowel MAT als circulerend adiponectin zijn ook verhoogd in vele andere voorwaarden, zoals het verouderen, oestrogeendeficiëntie en na behandeling met glucocorticoïden of anti-diabetische drugs (cijfer).4 maar zijn deze louter toevalligheden, of draagt MAT eigenlijk bij aan het doorgeven van adiponectin?
om deze vraag te beantwoorden, combineerden we klinische observaties met studies in een uniek muismodel dat bestand is tegen MATVORMING., Deze benaderingen toonden aan dat, tijdens calorische beperking,de MATUITBREIDING voor de volledige verhogingen van het doorgeven van adiponectin, 15 wordt vereist een conclusie aangezien gesteund door ons recenter onderzoek.4,13 de matuitbreiding tijdens calorie beperking schijnt ook metabolische aanpassingen binnen skeletachtige spier te beà nvloeden.15 het is onduidelijk of dit via adiponectin of andere endocriene factoren is, maar het onderstreept het potentieel van MAT om systemische gevolgen uit te oefenen.,
FUTURE MATTERS
de afgelopen tien jaar heeft het ontluikende gebied van MAT-onderzoek ons begrip van MATVORMING en-functie enorm verbeterd. MAT wordt niet langer beschouwd als een inerte’ ruimtevuller ‘ in het beenmerg, maar als een actief weefsel met uiteenlopende implicaties voor skelethermodellering, tumorprogressie, hematopoëtische regulatie en systemische endocriene en metabole functies. De studie van MAT blijft echter ver achter bij die van wat en BAT, en daarom moeten veel belangrijke vragen nog stevig worden beantwoord.,
gelukkig komt er nu een brede wetenschappelijke gemeenschap samen rond MAT-onderzoek. De eerste internationale bijeenkomst over BMA vond plaats in Lille, Frankrijk, in 2015, met succesvolle vervolgbijeenkomsten in 2016 en 2017. Op de 2017 BMA bijeenkomst in Lausanne, Zwitserland, de deelnemers gestemd voor de oprichting van de International Bone merg Adiposity Society, die gericht is op het bevorderen van de kennis van BMA (www.bma-society.org). deze ontwikkelingen benadrukken de toenemende interesse en enthousiasme voor de studie van MAT., Daarom kunnen we erop vertrouwen dat toekomstige onderzoeksinspanningen fundamentele kennis van MATBIOLOGIE zullen blijven ontsluiten, zowel als endocriene orgaan als daarbuiten.,William P Cawthorn, Chancellor ‘ s Fellow and MRC Career Development Fellow, University/British Heart Foundation Centre for Cardiovascular Science, University of Edinburgh, UK Ormond A MacDougald, John A Faulkner Collegiate Professor of Molecular and Integrative Physiology, University of Michigan Medical School, Ann Arbor, MI, USA anatomie &fysiologie 28 125-141.