deténgase y piense en sus huesos: ¿Qué imágenes vienen a la mente? Tal vez un cráneo con mandíbulas sonrientes, o las extremidades blancas fuertes que se extienden hacia los dedos de las manos y los pies. Incluso podría pensar en la médula ósea dentro de ellos, produciendo la sangre que corre a través de sus venas. Pero esto no es todo, porque tu esqueleto esconde un secreto: está lleno de grasa, y nadie sabe por qué.,
UN MISTERIO sin resolver
Este misterio sin resolver es sorprendente. Los científicos notaron por primera vez que nuestra médula ósea contiene células que almacenan grasa, llamadas adipocitos, hace más de un siglo.1 Tener adipocitos en nuestros huesos puede parecer inusual, pero no lo es: en los mamíferos, el tejido adiposo de la médula ósea (MAT) se desarrolla de manera constante después del nacimiento y se acumula rápidamente durante la pubertad, de modo que, cuando llegamos a la edad adulta, puede comprender hasta el 70% del volumen de la médula ósea, ¡esto representa más del 8% de la masa grasa total!,2
La estera no se distribuye uniformemente alrededor del esqueleto, sino que predomina en los brazos y las piernas. Esta estera periférica se desarrolla temprano después del nacimiento y rara vez se agota, y por lo tanto se ha denominado ‘estera constitutiva’ (cMAT).3 por el contrario, los sitios más centrales, como la columna vertebral, la pelvis y el esternón, así como las regiones más proximales de los huesos largos, contienen menos MAT y más médula roja hematopoyética (ver figura)., En estos sitios, los adipocitos de la médula son más difusos y tienden a aumentar o disminuir en respuesta a factores ambientales o patológicos; por lo tanto, este depósito se ha denominado ‘mat regulada’ (rMAT).3
otras propiedades de los adipocitos medulares también varían en estos sitios esqueléticos, con implicaciones potenciales para el impacto de la MAT en la salud y la enfermedad.2,3 de hecho, la MAT aumenta aún más con el envejecimiento y en diversas condiciones clínicas, incluidas las enfermedades esqueléticas, metabólicas y hematológicas (figura)., En consecuencia, el MAT está atrayendo un interés considerable como actor potencial en el desarrollo de numerosas enfermedades. Sin embargo, a diferencia de los tejidos adiposos blancos y marrones (WAT y BAT respectivamente), el estudio de MAT ha sido relativamente limitado. En consecuencia, las funciones fisiológicas y patológicas de la MAT siguen siendo poco conocidas.4 Entonces, ¿cuál es la función de la estera y cómo podría afectar la salud humana?
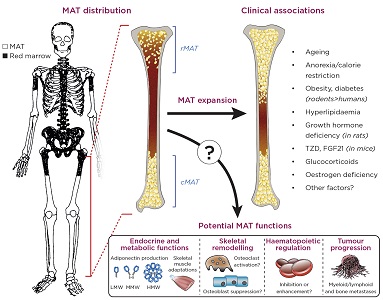
la distribución anatómica, las asociaciones clínicas y las funciones potenciales del tejido adiposo de la médula ósea (MAT)., La imagen del esqueleto está adaptada de Kricun (1985).16 cMAT: MAT constitutiva; rMAT: mat regulada; TZD: tiazolidindionas; FGF21: factor de crecimiento de fibroblastos 21; LMW/MMW/HMW: bajo/medio/alto peso molecular. Kricun me 1985 red-yellow marrow conversion: its effect on the location of some solitary bone lesions. Esquelético radiología 14(1), pp 10-19. ©Sociedad Esquelética Internacional 1985. Con permiso de Springer.
MALO HASTA EL HUESO?,
El aumento de la adiposidad de la médula ósea (BMA) se asocia con una menor densidad mineral ósea y un aumento de la fragilidad esquelética, por ejemplo en la osteoporosis, el envejecimiento y la deficiencia de estrógenos.5 Esto ha motivado la investigación sobre cómo MAT tiene un impacto en la integridad esquelética.
una posibilidad es que los adipocitos de la médula ósea compartan el mismo precursor de células madre esqueléticas que los osteoblastos formadores de hueso, en cuyo caso la acumulación de MAT podría ocurrir a expensas del desarrollo de osteoblastos.,6 Sin embargo, si bien esto es cierto durante el desarrollo embrionario, no está firmemente establecido si este precursor común persiste hasta la edad adulta para contribuir al mantenimiento del tejido postnatal.
otra posibilidad es que los adipocitos de la médula ósea secreten factores locales que perjudican directamente la formación ósea y / o estimulan la reabsorción ósea, aumentando así el riesgo de fractura.7 curiosamente, tales acciones paracrinas también podrían promover el crecimiento de tumores dentro del hueso, ya sean cánceres mieloides/linfoides primarios, o metástasis de otros lugares (figura).,8,9
por lo tanto, la acumulación de MAT es mala para la salud ósea? Desafortunadamente, es demasiado pronto para decirlo. Aunque el aumento de la MAT puede estar asociado con un riesgo elevado de fractura, el aumento de la MAT no siempre está asociado con la pérdida ósea. El impacto potencial de la MAT en el desarrollo del tumor esquelético también está por entenderse completamente. Dados los desafíos de Salud Pública que plantean la osteoporosis, los cánceres esqueléticos y las enfermedades asociadas al envejecimiento, dilucidar estas funciones de la MAT es un objetivo importante de la investigación en curso.,
Hematología
la función clave de la médula ósea está en la producción de células sanguíneas, por lo que no es sorprendente que muchos de los primeros estudios de MAT se llevaron a cabo desde una perspectiva hematológica. En general, la disminución de la MAT se asocia con un aumento de la hematopoyésis10, lo que sugiere un efecto supresor de la MAT.
apoyando esta posibilidad, un documento histórico de 2009 reveló que el bloqueo de la acumulación de MAT mejora la recuperación hematopoyética después del trasplante de médula ósea.,11 Esto tiene importantes implicaciones traslacionales: muchos receptores de trasplantes de médula ósea muestran una recuperación pobre a largo plazo, y por lo tanto la supresión de la adipogénesis de la médula podría representar un nuevo enfoque terapéutico.
sin embargo, no todos los datos apoyan un efecto negativo sobre la hematopoyesis. De hecho, investigaciones recientes sugieren que, en el contexto de los trasplantes de médula ósea, los adipocitos de médula segregan una molécula llamada factor de células madre, a través del cual promueven la hematopoyesis y la regeneración de las células madre hematopoyéticas.,12 así, en cuanto a los efectos putativos de la MAT sobre el hueso, su impacto en la hematopoyesis está demostrando ser más complejo de lo que se sospechaba (figura).
más allá del hueso: funciones metabólicas y endocrinas
aunque las funciones de MAT dentro del hueso y la médula están por establecerse de manera concluyente, parece claro que los adipocitos de la médula pueden influir en la homeostasis esquelética y la hematopoyesis secretando factores de acción local. Pero, ¿MAT, como WAT, también secreta productos endocrinos para ejercer efectos metabólicos sistémicos?
estudios Recientes de nuestros laboratorios y otros apoyan esta posibilidad., Numerosos informes muestran que los adipocitos de la médula ósea producen leptina, la hormona prototípica derivada de los adipocitos que tiene una gran influencia sobre la homeostasis energética, la inflamación y la función reproductiva.7 hemos encontrado que, al igual que en WAT, la expresión de leptina en MAT se suprime en respuesta a la disminución de la ingesta calórica,13 demostrando que MAT y WAT comparten mecanismos comunes para regular sus funciones endocrinas.
si la MAT contribuye a la leptina circulante sigue siendo desconocida, pero su función como fuente de otros factores endocrinos se está volviendo clara., Un foco importante de nuestra investigación ha estado en MAT como fuente de adiponectina, la otra hormona importante producida por el tejido adiposo. A pesar de esta fuente adiposa, la adiponectina circulante disminuye en la obesidad y aumenta en los estados de esbeltez, como durante la restricción calórica. Incluso después de 20 años de extensa investigación sobre la adiponectina, la base de esta llamada ‘paradoja de la adiponectina’ había permanecido incompleta; ¿por qué aumentaría una hormona derivada del tejido adiposo cuando falta WAT?
fue a través de esta lente que comenzamos a ver MAT bajo una nueva luz., En marcado contraste con WAT, la formación de MAT aumenta en estados de inanición, como durante la restricción calórica en animales y en pacientes humanos con anorexia nerviosa.14 tanto la MAT como la adiponectina circulante también aumentan en muchas otras condiciones, como el envejecimiento, la deficiencia de estrógenos y después del tratamiento con glucocorticoides o medicamentos antidiabéticos (figura).4 ¿pero son estas meras coincidencias, o el MAT realmente contribuye a la adiponectina circulante?
para responder a esta pregunta, combinamos observaciones clínicas con estudios en un modelo de ratón único que resiste la formación de MAT., Estos enfoques revelaron que, durante la restricción calórica, la expansión de la MAT es necesaria para los aumentos completos de la adiponectina circulante15,una conclusión que ya está respaldada por nuestra investigación más reciente.4,13 la expansión de la MAT durante la restricción calórica también parece influir en las adaptaciones metabólicas dentro del músculo esquelético.15 no está claro si esto es a través de adiponectina u otros factores endocrinos, pero subraya el potencial de MAT para ejercer efectos sistémicos.,
FUTURE MATTERS
durante la última década, el floreciente campo de investigación de MAT ha avanzado enormemente nuestra comprensión de la formación y función de MAT. El MAT ya no se considera un «relleno espacial» inerte dentro de la médula ósea, sino un tejido activo con diversas implicaciones para el remodelado esquelético, la progresión tumoral, la regulación hematopoyética y las funciones endocrinas y metabólicas sistémicas. Sin embargo, el estudio de MAT todavía está muy por detrás del de WAT y BAT, y por lo tanto muchas preguntas clave quedan por responder con firmeza.,
afortunadamente, una amplia comunidad científica se está uniendo en torno a la investigación MAT. El primer Encuentro Internacional sobre BMA se celebró en Lille, Francia, en 2015, con reuniones de seguimiento exitosas en 2016 y 2017. En la reunión de BMA 2017 en Lausana, Suiza, los asistentes votaron para establecer la Sociedad Internacional De Adiposidad de médula ósea, que tiene como objetivo avanzar en el conocimiento de BMA (www.bma-society.org). estos desarrollos ponen de relieve el creciente interés y entusiasmo por el estudio de MAT., Por lo tanto, podemos estar seguros de que los futuros esfuerzos de investigación continuarán para desbloquear el conocimiento fundamental de la biología de la MAT, tanto como órgano endocrino como más allá.,
William P Cawthorn, Chancellor’s Fellow y MRC Career Development Fellow, University/British Heart Foundation Centre for Cardiovascular Science, University of Edinburgh, UK
Muond a MacDougald, John a Faulkner Collegiate Professor of Molecular and Integrative Physiology, University of Michigan Medical School, Ann Arbor, MI, USA
- Muir R & Drummond WB 1893 Journal de anatomía & Fisiología 28 125-141.
- Scheller El et al. 2016 tendencias en Endocrinología & metabolismo 27 392-403.,
- Scheller El et al. 2015 Nature Communications 6 7808.
- Scheller El et al. 2016 Adipocyte 5 251-269.
- Schwartz AV 2015 fronteras en Endocrinología (Lausana) 6 40.
- Gimble JM et al. 1996 Bone 19 421-428.
- Sulston RJ & Cawthorn WP 2016 hormona Biología Molecular e Investigación Clínica 28 21-38.
- Shafat MS et al. 2017 Blood 129 1320-1332.
- Morris EV & Edwards CM 2016 Frontiers in Endocrinology (Lausanne) 7 90.
- Horowitz MC et al. 2017 adipocito 6 193-204.,
- Naveiras O et al. 2009 Nature 460 259-263.
- Zhou BO et al. 2017 Nature Cell Biology 19 891-903.
- Cawthorn WP et al. 2016 Endocrinología 157 508-521.
- Ghali O et al. 2016 fronteras en Endocrinología (Lausana) 7 125.
- Cawthorn WP et al. 2014 Metabolismo Celular 20 368-375.
- Kricun me 1985 Radiología esquelética 14 10-19.