INNLEDNING
Anti-glomerular basalmembran antistoff sykdom er en immunologisk lidelse preget av tilstedeværelsen av sirkulerende antistoffer som virker direkte mot en iboende antigen av glomerular basalmembran, provoserte en hurtig progredierende glomerulonefritt (RPGN).,
Goodpasture ‘ s syndrom (GPS) har generelt vært brukt som et synonym for anti-glomerular basalmembran antistoff sykdom, som er karakterisert ved sammenslutning av RPGN og alveolar blødning i nærvær av anti-basalmembran antistoffer (anti-BM Ab). Skade på sentralnervesystemet (CNS) fra GPS er ganske sjeldne i fravær av anti-nøytrofile cytoplasma antistoffer (ANCA), og har bare blitt beskrevet i 4 tilfeller i medisinsk litteratur.,1-4
Her presenterer vi tilfelle av en 20 år gammel pasient som startet med RPGN, ledsaget av haemoptoic sputum og to episoder av generalisert tonic-clonic krampaktige anfall, med høy anti-BM Ab titre.
Kliniske saken
20-år gammel mann, røyker og tidligere kokain og cannabis brukeren, som ble innlagt på sykehus med makroskopiske haematuria og akutt oliguric nyresvikt (AORF)., 12 dager før opptak, pasienten presentert med asthenia, anoreksi, oppkast, og dysuri, for som han besøkte en allmennlege som diagnostisert ham med en urinveisinfeksjon og foreskrevet ciprofloxacin behandling. Fire dager senere, han henviste feber over 38 º c, makroskopiske haematuria, og en subjektiv nedgang i diurese.
Den fysiske undersøkelsen avdekket følgende: blodtrykk: 140/90 mmHg, temperatur: 37 ºC. Forverret helse, blekhet i huden, og mucosae, og bibasal hypoventilation., Ved opptak, AORF ble observert, krever hemodialyse i løpet av de første 24 timer. 48 timer senere, pasienten presentert haemoptoic sputum, etterfulgt av to episoder av generell tonic-clonic krampaktige anfall.
Fire dager etter at pasienten ble innlagt, har vi utført en percoetaneous nedsatt biopsi, der vi observert en extracapillary glomerulonefritt (100% av crescents), med kollapset glomerular tufts, områder med fibrinoid nekrose, moderat inflammatorisk infiltrasjon og begynnende interstitiell fibrose og tubulær atrofi (Figur 1)., Den immunfluorescens skanningen viste lineær forekomster av immunglobulin G (IgG) langs glomerular basalmembran.
pasienten ble diagnostisert med GPS forbundet med en sannsynlig ANCA negative CNS vaskulitt. Ved opptak, pasienten ble behandlet med 3 500mg boluses av metylprednisolon i 3 påfølgende dager. Senere, muntlig cyclophosphamide ble lagt i en daglig dose på 1,5 mg/kg sammen med 15 økter med plasmaferese. Videre, pasienten har mottatt behandling med valproinsyre., I luftveiene og nevrologiske symptomer forsvant med den foreskrevne behandling, men dessverre, nyrefunksjon ikke gjenopprette, og pasienten fortsatt på en hemodialyse program ved avslutning.
Tjue fem dager etter å ha blitt tillatt, pasienten ble utskrevet fra sykehuset med negativ anti-BM Ab titre, slik at en langsom reduksjon i immunsuppressiv behandling, med ingen indikasjoner på tilbakefall. Cyclophosphamide ble avsluttet 3 måneder etter opptak, men pasienten fortsatt på lave doser av steroider (2,5 mg/dag) og på en hemodialyse program (Figur 2).,
Påfølgende utviklingen
Seks måneder etter å ha blitt sluppet ut, og etter ikke-samsvarskrav for antihypertensive behandlingen, pasienten var readmitted for en hypertensiv krise (blodtrykk på 220/120 mmHg og en rett timelige intraparenchymal haematoma som krevde kirurgisk drenasje). På dette punktet, serielle målinger av anti-BM Ab nivåer var negative, og på tross av alvorlighetsgraden av skaden, pasienten presentert med ingen nevrologiske underskudd ved avslutning.,
Tjue måneder senere, har pasienten mottatt en nyretransplantasjon fra et organ donor, så vel som immunsuppressiv behandling med takrolimus, mycophenolate mofetil, og prednisone. Den nyretransplantasjon har vært tilfredsstillende så langt, og pasienten har vist ingen tilbakefall av sykdommen (Tabell 1).
DISKUSJON
GPS er en sjelden immunologiske lidelse preget av triaden av RPGN, tilstedeværelse av sirkulerende anti-BM Ab, og pulmonal blødning., Selv om genetiske faktorer har vært forbundet med en økt sannsynlighet for å utvikle denne syndrom, andre faktorer som miljø-eksponering (viral infeksjoner, eksponering for flyktige hydrokarboner og tobakk røyk) kan utløse sykdom hos predisponerte individer, særlig i de med underliggende pulmonal lesjoner.5 i Tillegg, forbruket av kokain har også vært i slekt å anti-BM Ab sykdom.6 Vår pasient var en røyker, så vel som en tidligere bruker kokain, faktorer som kan ha påvirket på å utløse sykdommen.,
I 10 til 30% av tilfellene, anti-BM Ab sykdom er assosiert med ANCA, og de fleste av pasientene har lave titre av anti-myeloperoxidase (MPO). Denne undergruppen av pasienter sannsynligvis presenterer en variant av forbundet vaskulitt.7 Imidlertid, selv om den eksakte årsaken til utvikling av ANCA i anti-BM Ab sykdom ikke har vært avklart, noen forfattere foreslår at en polyklonal aktivering mekanisme kan være ansvarlig for.8
GPS-er preget av tilstedeværelsen av autoantistoffer mot epitope av alfa-3-kjeden av type IV kollagen (alfa-3 NCI), kalt Goodpasture antigen.,9 Selv om dette antigenet har en bred distribusjon, det er først og fremst uttrykt i glomerular og alveolar kjelleren membraner, og sjeldnere i rørformet, cochlear, retinal, og årehinnen plexus kjelleren membraner.
Cerebral engasjement i GPS er ekstremt sjeldne i fravær av ANCA, og bare 4 saker som har vært beskrevet i den medisinske litteraturen.1-4 Alle saker som har blitt kommunisert presentert med tilbakevendende krampaktige anfall i slekt å cerebral vaskulitt med eller uten haemoptysis. Rydel et al.,1 beskrevet det første tilfellet av ANCA-negativ cerebral vaskulitt forbundet med GPS, som viser vasculitic infiltrerer i meningeal biopsi. Selv om cerebral og meningeal biopsi utgjør gullstandard for diagnosen cerebral vaskulitt, deres bruk er i dag begrenset til pasienter med tvilsomt diagnose på grunn av den aggressive natur prosedyre., Videre, i de fleste av de som er beskrevet tilfeller av GPS med cerebral engasjement, diagnosene av ANCA-negativ cerebral vaskulitt forbundet med GPS ble utført basert på klinisk undersøkelse av pasienten og funn fra imaging tester.2-4 Vår pasient i gang med RPGN som krever dialyse fra begynnelsen, etterfulgt av pulmonal blødning og to hendelser av tonic-clonic krampaktige anfall, sammen med forhøyet anti-BM Ab nivåer., Gjentatte ANCA målinger var negative, og andre mulige årsaker som kan ha utløst den krampaktige anfall, for eksempel metabolske forstyrrelser, bedøve nød-indusert hypertensive beslag, etc. ble ekskludert. Selv om cerebral MR kom opp vanlig i vår pasient, vi kan ikke utelukke at små fartøy vasculitic lesjoner kan ha bidratt til den cerebrale skader som ble påført. Faktisk, cerebral MR skanner komme opp negative i så mye som 35% av pasienter med cerebral vaskulitt.,10 Cerebral angiografi ble ikke utført fordi den nevrologiske symptomer forsvant med det som er beskrevet tidligere behandling. Videre har vi også observert en forbedring i respiratoriske symptomer, selv om nyrefunksjon aldri utvinnes. Levy et al. viste at nedsatt nyrefunksjon som anslått av plasma kreatinin-nivåene (>5.7 mg/dL) eller behovet for dialyse ved utbruddet av sykdommen, så vel som en andel som er større enn 50% av crescents funnet i nedsatt biopsi, er alle negative prognostiske faktorer for utvinning av nyrefunksjon.,11
Nyre-transplantasjon er det mulig å gjennomføre denne sykdommen, selv om det ikke eksisterer en risiko for tilbakefall i nytt orgel, som fører til anbefaling at minst en 6-måneders ventetid være nødvendig for transplantasjon, og bare når anti-BM Ab titre er umulig å oppdage. Dette er en lovende strategi i de fleste tilfeller, som hos vår pasient, som fikk et organ donor transplantasjon 20 måneder senere, presenterer med en positiv klinisk utvikling, og ingen tegn til tilbakefall av sykdommen.,
til Slutt, kan vi konkludere med at GPS med nevrologiske engasjement er svært sjeldne, spesielt med negative ANCA. Normal cerebral MR funn ikke utelukke muligheten av små fartøy cerebral vaskulitt, som krever en aggressiv og tidlig diagnose og behandling av GPS for å forbedre prognosen til pasienten.
TAKK
forfatterne ønsker å takke Dr. Eduardo Salido for hans råd om nedsatt patologi og gjennomgang av manuskriptet.
– >
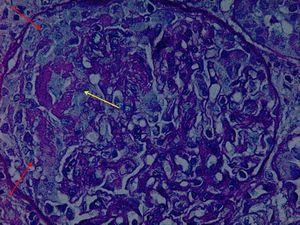
Figur 1., Extracapillary glomerulonefritt (røde piler) med sentre for fibrinoid nekrose. Gul pil, PAS flekken, 400x.