촉매은 물질 속도가 빨라지는 화학 반응하지만,소비되지 않으로 반응한다;따라서 촉매를 복구할 수 있는 화학적으로 변화에 반응이 끝나면 그것이 사용되었을 속도,또는 촉매.

토론
화학 물질에 대한 반응하는,그 채권해야 합 다시 정렬하기 때문에 유대에서 제품에서 다른 사람들에 반응.,가장 느린 단계에서 채권 재배열을 생산하이 무엇이라고 불리 전환 상태는 화학 종는지 반응 또는 제품이지만,중간 사이에 두.
에너지 필요한 형태로 전환 상태입니다. 이 에너지를 활성화 에너지 또는 Ea 라고합니다.아래 다이어그램을 왼쪽에서 오른쪽으로 읽으면 반응물이 전이 상태를 통과하여 생성물이됨에 따라 반응의 진행이 표시됩니다.,
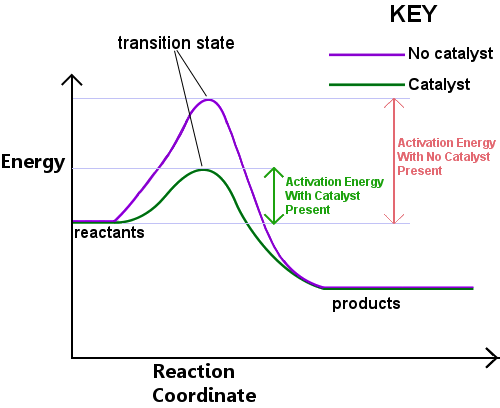
활성화 에너지 생각할 수 있습의 장벽으로 화학 반응,장애물이 교차 해야 합니다.는 경우에 장벽이 높고,몇 분자가 충분한 운동 에너지,충돌 형태로 전환 상태,그리고 십자가입니다.Ea 보다 낮은 에너지를 갖는 반응물은 전이 상태를 통과하여 반응하여 생성물이 될 수 없다.
촉매는 반응에 대해 더 낮은 Ea 와 함께 다른 경로를 제공함으로써 작동합니다. 촉매는 에너지 장벽을 낮춘다.,다양한 경로를 할 수 있습 유대인정보취급방침 변환하는 데 필요 반응물 제품을 더 쉽게,더 낮은 에너지 입력이 있습니다.에서 지정된 시간 간격,촉매의 존재할 수 있습 큰 비율 반응의 종을 선택한 충분한 에너지를 전달을 통한 전이 상태가 될 제품입니다.
예제 1:Haber 과정
하버 프로세스를 만들기 위해 사용되는 암모니아에서의 수소 및 질소,촉매에 의해 철 제공하는 원자 사이트에서는 반응물질 채권을 다시 정렬 할 수 있습니다 더 형성하기 위하여 쉽게 전환 상태입니다.,
예제 2:효소
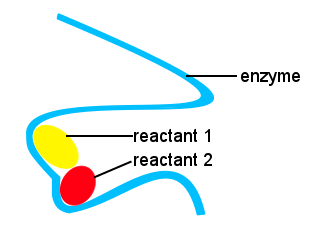
에서 우리 몸에서,그리고 다른 살아있는 것,효소의 속도를 이용하는 생화학 반응입니다. 효소는 촉매의 한 유형입니다.반응이 적당한 속도로 일어나도록 효소 없이는 복잡한 삶이 불가능할 것입니다.의 모양에 따라 효소의 위치와에서 효소 바인딩하는 반응물은 대안을 제공합 반응이 통로 허용,특정한 분자들이 함께하는 형태로 전환 상태로 감소 활성화 에너지 장벽이 있습니다.,
에서도 아래,장기 체인을 효소 제공하는 사이트를 위한 분자 반응을 형성하기 위해 함께 전환 상태로 저렴한 활성화 에너지입니다.
촉매제할 수 없는 변화의 위치를 화학 평형-전후의 반응은 모두 가속도록 균형을 일정한 Keq 변경되지 않습니다.그러나 제거하여 제품에서 반응 혼합물을 형성으로,전반적인 비율의 제품을 형성할 수 있습에서 연습할 수 있습니다.