La termodinamica è una branca della fisicache si occupa dell’energia e del lavoro di un sistema.La termodinamica si occupa solo della grande risposta di scala di un sistema che possiamo osservare e misurare in esperimenti. Le interazioni di gas su piccola scala sonodescritto dalla teoria cinetica dei gas.Ci sono tre principalileggi della termodinamica che sono descritti su diapositive separate., Ogni legge porta alla definizione diproprietà termodinamiche che ci aiutano a comprendere e prevedere il funzionamento di un sistema fisico. Presenteremo alcuni semplici esempi di queste leggi e proprietà per una varietà di sistemi fisici, sebbene siamo più interessati alla termodinamica dei sistemi di propulsione e ai flussi ad alta velocità.Fortunatamente, molti degli esempi classici di termodinamica coinvolgono la dinamica del gas.,
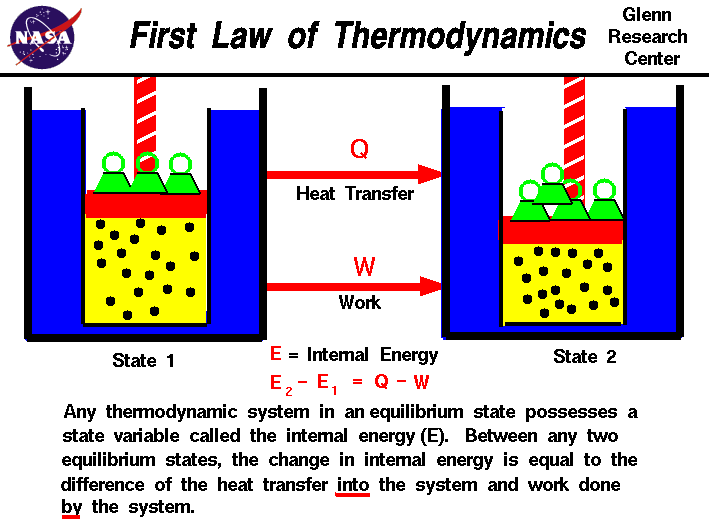
Nelle nostre osservazioni sul lavoro svolto su,o da un gas, abbiamo scoperto che la quantità di lavoro dipende non solo dagli stati iniziali e finali del gasma anche dal processo, o percorso che produce lo stato finale.Allo stesso modo la quantità di calore trasferito in, orfrom un gas dipende anche dagli stati iniziale e finale e theprocess che produce lo stato finale., Molte osservazioni di realgas hanno dimostrato che la differenza del flusso di calore nel gase il lavoro svolto dal gas dipende solo dagli stati iniziali e finalistati del gas e non dipende dal processo o dal percorso che produce lo stato finale. Questo suggerisce l’esistenza di anovariabile aggiuntiva, chiamata energia interna del gas,che dipende solo dallo stato del gas e non da alcun processo.L’energia interna è una variabile di stato, proprio come la temperatura o la pressione., La prima legge della termodinamica definisce l’internoenergia (E) uguale alla differenza del trasferimento di calore (Q) inun sistema e il lavoro (W) svolto dal sistema.
E2 – E1 = Q – W
Abbiamo sottolineato le parole “into” e “by” nella definizione. Calore rimosso da un sistemasarebbe assegnato un segno negativo nell’equazione. Allo stesso modo workdone sul sistema viene assegnato un segno negativo.,
L’energia interna è solo una forma di energia come l’energia potenziale di un oggetto ad una certa altezza sopra la terra, o l’energia cinetica di un oggetto in movimento. Allo stesso modo in cui l’energia potenziale può essere convertita in energia cinetica conservando l’energia totale del sistema, l’energia interna di un sistema termodinamico può essere convertita in energia cinetica o potenziale. Come potentialenergy, l’energia interna può essere immagazzinata nel sistema.Si noti, tuttavia, che il calore e il lavoro non possono essere conservati o conservati in modo indipendente poiché dipendono dal processo., La prima legge della termodinamica consente l’esistenza di molti stati possibili di un sistema, ma solo alcuni stati sono trovati in natura. La seconda legge della termodinamica aiuta a spiegare questa osservazione.
Se un sistema è completamente isolato dall’ambiente esterno, è possibile avere un cambiamento di stato in cui nessun calore viene trasferito nel sistema. Gli scienziati si riferiscono a un processo che non comporta il trasferimento di calore come un processo adiabatico.,L’implementazione della prima legge della termodinamica per i gas ne introduce un’altravariabile di stato utile chiamata entalpiche è descritto in una pagina separata.
Attività:
Visite guidate
 Termodinamica:
Termodinamica: 
Navigazione ..
![]()
![]()
![]()
Guida per principianti Home Page