The chemical element hafnium is classed as a transition metal . It was discovered in 1923 by Georg von Hevesy and Dirk Coster.

Data Zone
| Classification: | Hafnium is a transition metal |
| Color: | silvery |
| Atomic weight: | 178.,49 |
| State: | solid |
| Melting point: | 2230 oC, 2503 K |
| Boiling point: | 4600 oC, 4873 K |
| Electrons: | 72 |
| Protons: | 72 |
| Neutrons in most abundant isotope: | 108 |
| Electron shells: | 2,8,18,32,10,2 |
| Electron configuration: | 4f14 5d2 6s2 |
| Density @ 20oC: | 13.,2 g/cm3 |
Show more, including: Heats, Energies, Oxidation,
Reactions, Compounds, Radii, Conductivities
| Atomic volume: | 13.6 cm3/mol |
| Structure: | hcp: hexagonal close pkd |
| Hardness: | 5.5 mohs |
| Specific heat capacity | 0.14 J g-1 K-1 |
| Heat of fusion | 27.2 kJ mol-1 |
| Heat of atomization | 621 kJ mol-1 |
| Heat of vaporization | 575.,0 kJ mol-1 |
| 1st ionization energy | 658.5 kJ mol-1 |
| 2nd ionization energy | 1440 kJ mol-1 |
| 3rd ionization energy | 2250 kJ mol-1 |
| Electron affinity | 178 kJ mol-1 |
| Minimum oxidation number | 0 |
| Min. common oxidation no. | 0 |
| Maximum oxidation number | 4 |
| Max. common oxidation no. | 4 |
| Electronegativity (Pauling Scale) | 1.,3 |
| Volume di polarizzabilità | 16.,none |
| Oxide(s) | HfO2 |
| Hydride(s) | HfH2 |
| Chloride(s) | HfCl4 |
| Atomic radius | 155 pm |
| Ionic radius (1+ ion) | – |
| Ionic radius (2+ ion) | – |
| Ionic radius (3+ ion) | – |
| Ionic radius (1- ion) | – |
| Ionic radius (2- ion) | – |
| Ionic radius (3- ion) | – |
| Thermal conductivity | 23.,2 W m-1 K-1 |
| conducibilità Elettrica | 3.4 x 106 S m-1 |
| di Congelamento punto di Fusione: | 2230 oC, 2503 K |

Afnio è un metallo di colore argento. Normalmente appare piuttosto grigio a causa dello strato di ossido che si forma nell’aria. La polvere di afnio, senza lo strato di ossido, può accendersi spontaneamente nell’aria. Immagine Rif., (1)
La scoperta dell’afnio
L’esistenza dell’afnio fu originariamente prevista dal chimico russo Dmitri Mendeleev. Nel suo libro del 1869 “The Periodic Law of the Chemical Elements” predisse l’esistenza di un elemento con proprietà simili a, ma più pesante del titanio e dello zirconio.
Nel 1911, Georges Urbain, lo scopritore del lutezio delle terre rare, pensò di aver scoperto l’elemento 72 durante la sua analisi spettrale delle terre rare. Chiamò questo nuovo elemento celtium, ma tre anni dopo si dimostrò essere una miscela di lantanidi già scoperti., (2)
Nel 1921, Neils Bohr suggerì al chimico ungherese Georg von Hevesy di cercare l’elemento mancante nei minerali di zirconio. (3) Secondo la teoria quantistica della struttura atomica di Bohr, questi metalli avrebbero proprietà chimiche simili, quindi c’era una buona probabilità che si trovassero negli stessi minerali.
Seguendo il consiglio di Bohr, Hevesy e il fisico olandese Dirk Coster scoprirono l’afnio nel 1923 usando la spettroscopia a raggi X per analizzare i minerali di zirconio.
Anton Eduard van Arkel e Jan Hendrik de Boer scoprirono un metodo per produrre afnio ad alta purezza nel 1925., Il tetraioduro di afnio (HfI4) viene decomposto su un filamento di tungsteno caldo bianco creando una barra di cristallo di afnio puro. Questo è noto come il processo di barra di cristallo.
L’elemento era chiamato Afnio dal nome latino ‘Hafnia’, che significa Copenaghen, la città in cui l’elemento è stato scoperto.

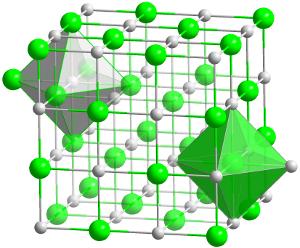
struttura di Cristallo del carburo di afnio (HfC)., Questo è il composto più refrattario (resistente al calore) noto di due elementi in rapporto 1:1.

L’afnio è usato nelle barre di controllo dei reattori nucleari nei sottomarini nucleari

Bianco ossido di afnio (IV) (HfO2). Composti a base di ossido di afnio vengono introdotti nei chip di silicio per produrre processori più piccoli e ad alte prestazioni con una migliore efficienza energetica.,
Aspetto e caratteristiche
Effetti nocivi:
L’afnio è considerato non tossico. In forma in polvere è piroforico (può accendersi spontaneamente).
Caratteristiche:
L’afnio è un metallo brillante, argenteo e duttile.
Chimicamente è simile allo zirconio.
Quando presente nei composti, l’afnio esiste principalmente nello stato di ossidazione IV.
L’afnio resiste alla corrosione a causa della formazione di un film di ossido sulle superfici esposte.
Non è influenzato da tutti gli acidi (a parte il fluoruro di idrogeno) e da tutti gli alcali.,
L’afnio reagisce con gli alogeni per formare tetraalidi e ad alte temperature reagisce con carbonio, boro, azoto, ossigeno, silicio e zolfo.
Usi dell’afnio
L’afnio viene utilizzato per le barre di controllo dei reattori nucleari a causa della sua capacità di assorbire i neutroni e delle sue buone qualità meccaniche e di resistenza alla corrosione. Questo è in completo contrasto con lo zirconio, che sebbene sia chimicamente molto simile all’afnio, è molto povero nell’assorbire i neutroni., Lo zirconio viene quindi utilizzato nel rivestimento (strato esterno) delle barre di combustibile attraverso le quali è importante che i neutroni possano viaggiare facilmente.
L’afnio viene utilizzato anche nelle lampadine flash fotografiche, nei filamenti delle lampadine e nelle apparecchiature elettroniche come catodi e condensatori.
Leghe di afnio con molti altri metalli, come ferro, niobio, tantalio e titanio.
Le leghe di afnio-niobio, ad esempio, sono resistenti al calore e vengono utilizzate in applicazioni aerospaziali, come i motori a razzo spaziale.,
Il carburo di afnio è utilizzato per allineare forni / forni ad alta temperatura grazie alle sue proprietà refrattarie (non si scioglie ad alte temperature).
I composti a base di afnio sono utilizzati negli isolatori di gate nella generazione di circuiti integrati a 45 nm per computer.
I composti a base di ossido di afnio vengono introdotti nei chip a base di silicio per produrre processori più piccoli, più efficienti dal punto di vista energetico e con prestazioni elevate(4).
Abbondanza e isotopi
Abbondanza crosta terrestre: 3,3 parti per milione in peso, 0.,4 parti per milione da moli
Abbondanza sistema solare: 1 parte per miliardo in peso, 0,01 parti per miliardo da moli
Costo, puro: pure 120 per 100g
Costo, massa: per per 100g
Fonte: L’afnio non si trova libero in natura ma si trova nella maggior parte dei minerali di zirconio ad una concentrazione compresa tra Commercialmente, l’afnio è prodotto come sottoprodotto della raffinazione dello zirconio. Questo viene fatto usando il processo Kroll, riducendo il tetracloruro con magnesio o con sodio.,

- Foto di Deglr6328
- Per Enghag, Enciclopedia degli Elementi: Dati Tecnici – Storia – di Elaborazione di Applicazioni Del 2008, John Wiley & Figli, p527.
- Bob Weintraub, George De Hevesy (1885 1966) (documento pdf).
- Aile Tamm, Atomic Layer Deposition Of High-Permittivity Isolators From Cyclopentadienyl-Based Precursors, 2010, Tartu University Press, p18.,
Citare questa Pagina
Per la linea di collegamento, si prega di copiare e incollare uno dei seguenti:
<a href="https://www.chemicool.com/elements/hafnium.html">Hafnium</a>
o
<a href="https://www.chemicool.com/elements/hafnium.html">Hafnium Element Facts</a>
Per citare questa pagina accademica documento, si prega di utilizzare il seguente MLA conforme citazione:
"Hafnium." Chemicool Periodic Table. Chemicool.com. 17 Oct. 2012. Web. <https://www.chemicool.com/elements/hafnium.html>.