Un acétal est un groupe fonctionnel avec la connectivité R2C(OU’)2). Ici, les groupes R peuvent être des fragments organiques (un atome de carbone, avec d’autres atomes arbitraires attachés à celui-ci) ou de l’hydrogène, tandis que les groupes R’ doivent être des fragments organiques et non de l’hydrogène. Les deux groupes R ‘peuvent être équivalents l’un à l’autre (un » acétal symétrique ») ou non (un »acétal mixte »)., Les acétals sont formés à partir et convertibles en aldéhydes ou cétones et ont le même état d’oxydation au niveau du carbone central, mais ont une stabilité chimique et une réactivité sensiblement différentes par rapport aux composés carbonyles analogues. L’atome de carbone central a quatre liaisons avec lui, et est donc saturé et a une géométrie tétraédrique.,

structure générique des acétals
le terme cétal est parfois utilisé pour identifier les structures associées aux cétones (les deux groupes R Les fragments organiques plutôt que l’hydrogène) plutôt que les aldéhydes et, historiquement, utilisé spécifiquement pour les cas liés à l’aldéhyde (ayant au moins un hydrogène à la place d’un r sur le carbone central). L’IUPAC a à l’origine déconseillé l’utilisation du mot ketal, mais est depuis revenue sur sa décision., Cependant, contrairement à l’utilisation historique, les cétals sont maintenant un sous-ensemble des acétals, un terme qui englobe maintenant les structures dérivées de l’aldéhyde et de la cétone.
Si L’un des groupes R a un oxygène comme premier atome (c’est-à-dire qu’il y a plus de deux oxygènes liés au carbone central), le groupe fonctionnel est plutôt un orthoester. Contrairement aux variations de R, Les deux groupes R’ sont des fragments organiques. Si un R ‘ est un hydrogène, le groupe fonctionnel est plutôt un hémiacétal, tandis que si les deux sont H, le groupe fonctionnel est un hydrate de cétone ou un hydrate d’aldéhyde.,
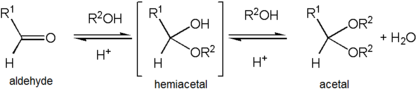
la Formation d’un acétal se produit lorsque le groupe hydroxyle d’un hémiacétal devient protoné et est perdu sous forme d’eau. Le carbocation qui est produit est alors rapidement attaqué par une molécule d’alcool. La perte du proton de l’alcool attaché donne l’acétal.,
Acetals are stable compared to hemiacetals but their formation is a reversible equilibrium as with esters., En réaction à la création d’un acétal, l’eau doit être retirée du mélange réactionnel, par exemple avec un appareil Dean–Stark, de peur qu’il n’hydrolyse le produit dans l’hémiacétal. La formation d’acétals réduit le nombre total de molécules présentes (carbonyle + alcool 2 → acétal + eau) et n’est donc généralement pas favorable en ce qui concerne l’entropie. Une situation où il n’est pas entropiquement défavorable est lorsqu’une seule molécule de diol est utilisée plutôt que deux molécules d’alcool distinctes (carbonyle + diol → acétal + eau)., Une autre façon d’éviter le coût entropique est d’effectuer la synthèse par échange acétal, en utilisant un réactif de type acétal préexistant comme donneur du groupe OR’plutôt qu’une simple addition d’alcools eux-mêmes. Un type de réactif utilisé pour cette méthode est un orthoester. Dans ce cas, l’eau produite avec le produit acétal est détruite lorsqu’elle hydrolyse les molécules d’orthoester résiduelles, et cette réaction secondaire produit également plus d’alcool à utiliser dans la réaction principale.,
les acétals sont utilisés comme groupes protecteurs pour les groupes carbonyle en synthèse organique car ils sont stables par rapport à l’hydrolyse par les bases et par rapport à de nombreux agents oxydants et réducteurs. Ils peuvent protéger le carbonyle dans une molécule (temporairement par la réaction avec un alcool) ou un diol (temporairement par la réaction avec un carbonyle). C’est-à-dire que soit le carbonyle, soit les alcools, ou les deux pourraient faire partie de la molécule dont la réactivité doit être contrôlée.
divers composés carbonyles spécifiques ont des noms spéciaux pour leurs formes acétales., Par exemple, un acétal formé à partir de formaldéhyde (deux hydrogènes attachés au carbone central) est parfois appelé un groupe formel ou le groupe méthylènedioxy. L’acétal formé à partir d’acétone est parfois appelé acétonide.