en acetal är en funktionell grupp med anslutning R2C(eller’)2). Här kan R-grupperna vara organiska fragment (en kolatom, med godtyckliga andra atomer kopplade till det) eller väte, medan R-grupperna måste vara organiska fragment inte väte. De två R-grupperna kan vara likvärdiga med varandra (en” symmetrisk acetal”) eller inte (en”blandad acetal”)., Acetaler är bildade från och konvertibla till aldehyder eller ketoner och har samma oxidationstillstånd vid det centrala kolet, men har väsentligt olika kemisk stabilitet och reaktivitet jämfört med de analoga karbonylföreningarna. Den centrala kolatomen har fyra bindningar till den, och är därför mättad och har tetrahedral geometri.,

Generisk struktur av acetaler
termen ketal används ibland för att identifiera strukturer som är associerade med ketoner (båda R-grupperna organiska fragment snarare än väte) snarare än aldehyder och, historiskt sett, termen acetal användes specifikt för aldehydrelaterade fall (med minst en väte i stället för en R på det centrala kolet). IUPAC föråldrade ursprungligen användningen av ordet ketal helt och hållet, men har sedan dess ändrat sitt beslut., Men i motsats till historisk användning är ketaler nu en delmängd av acetaler, en term som nu omfattar både aldehyd – och keton-härledda strukturer.
om en av R-grupperna har ett syre som den första atomen (det vill säga det finns mer än två oxygenerbundna till det centrala kolet) är den funktionella gruppen istället en ortoester. I motsats till variationer av R är båda R-grupperna organiska fragment. Om en R’ är ett väte, den funktionella gruppen är istället en hemiacetal, medan om båda är H, den funktionella gruppen är en ketonhydrat eller aldehydhydrat.,
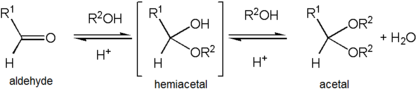
bildandet av en acetal inträffar när hydroxylgruppen av en hemiacetal blir protonerad och förloras som vatten. Den karbokation som produceras attackeras sedan snabbt av en alkoholmolekyl. Förlust av proton från den bifogade alkoholen ger acetal.,
Acetals are stable compared to hemiacetals but their formation is a reversible equilibrium as with esters., Som en reaktion för att skapa en acetal fortsätter, måste vatten avlägsnas från reaktionsblandningen, till exempel med en Dean–Stark apparat, så att den hydrolyserar produkten tillbaka till hemiacetalen. Bildandet av acetaler minskar det totala antalet molekyler som finns (karbonyl + 2 alkohol → acetal + vatten) och är därför i allmänhet inte gynnsamt med avseende på entropi. En situation där den inte är entropiskt ogynnsam är när en enda diolmolekyl används snarare än två separata alkoholmolekyler (karbonyl + diol → acetal + vatten)., Ett annat sätt att undvika den entropiska kostnaden är att utföra syntesen genom acetalutbyte, med hjälp av ett redan existerande acetal-typreagens som eller’-gruppdonator snarare än enkel tillsats av alkoholer själva. En typ av reagens som används för denna metod är en ortoester. I detta fall förstörs vatten som produceras tillsammans med acetalprodukten när det hydrolyserar resterande ortoestermolekyler, och denna sidoreaktion producerar också mer alkohol som ska användas i huvudreaktionen.,
acetaler används som skyddsgrupper för karbonylgrupper i organisk syntes eftersom de är stabila med avseende på hydrolys av baser och med avseende på många oxiderande och reducerande medel. De kan antingen skydda karbonylen i en molekyl (genom att tillfälligt reagera den med en alkohol) eller en diol (genom att tillfälligt reagera den med en karbonyl). Det vill säga antingen karbonylen eller alkoholerna, eller båda kan vara en del av molekylen vars reaktivitet ska kontrolleras.
olika specifika karbonylföreningar har speciella namn för deras acetalformer., Till exempel kallas en acetal bildad av formaldehyd (två hydrogener kopplade till det centrala kolet) ibland en formell eller metylendioxi-gruppen. Den acetal som bildas av aceton kallas ibland en Acetonid.