Termodynamika jest gałęzią fizyki, która zajmuje się energią i pracą układu.Termodynamika dotyczy tylko dużej skali reakcji układu, którą możemy obserwować i mierzyć w eksperymentach. Oddziaływania gazów w małej skali są opisywane przez kinetyczną teorię gazów.Istnieją trzy podstawowe zasady termodynamiki, które są opisane na oddzielnych szkiełkach., Każdy z nich prowadzi do zdefiniowania właściwości termodynamicznych, które pomagają nam zrozumieć i przewidzieć działanie układu fizycznego. Przedstawimy kilka prostych przykładów tych praw i zalet dla różnych układów fizycznych, chociaż najbardziej interesuje nas Termodynamika układów napędowych i przepływy o dużej prędkości.Na szczęście wiele przykładów termodynamiki wiąże się z dynamiką gazu.,
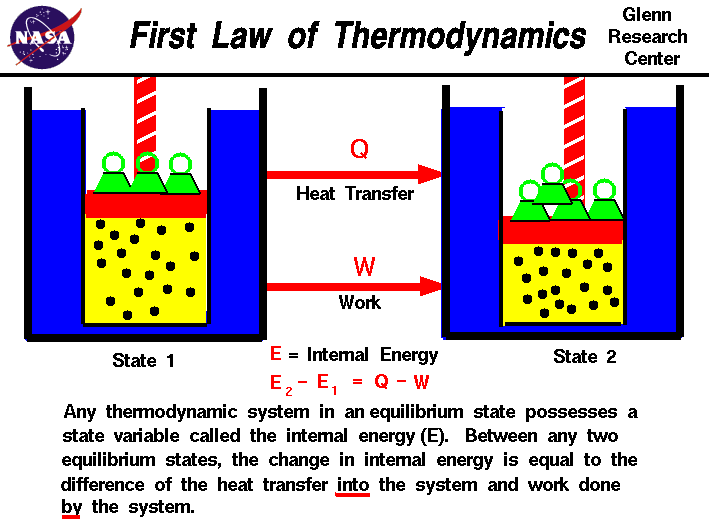
w naszych obserwacjach pracy wykonanej na gazie lub za pomocą gazu,odkryliśmy, że ilość pracy zależy nie tylko od początkowych i końcowych Stanów gazu, ale także od procesu lub ścieżki, która wytwarza stan końcowy.Podobnie ilość ciepła przenoszonego do lub z gazu zależy również od stanu początkowego i końcowego oraz procesu, który wytwarza stan końcowy., Wiele obserwacji gazów rzeczywistych wykazało, że różnica przepływu ciepła do gazu i praca wykonywana przez gaz zależy tylko od początkowych i końcowych Stanów gazu i nie zależy od procesu lub ścieżki, która wytwarza stan końcowy. Sugeruje to istnienie zmiennej dodatkowej, zwanej energią wewnętrzną gazu, która zależy tylko od stanu gazu, a nie od żadnego procesu.Energia wewnętrzna jest zmienną stanu, podobnie jak temperatura czy ciśnienie., Pierwsze prawo termodynamiki definiuje energię wewnętrzną (E) jako równą różnicy przenikania ciepła (Q) do układu i pracy (W) wykonywanej przez układ.
E2 – E1 = Q – W
w definicji podkreśliliśmy słowa „do” i „przez”. Ciepło usuwane z układu powinno być przypisane znakowi ujemnemu w równaniu. Podobnie w systemie przypisany jest znak ujemny.,
energia wewnętrzna jest tylko formą energii, jak potencjalenergy obiektu na pewnej wysokości nad ziemią, lub kineticenergy obiektu w ruchu. W ten sam sposób, w jaki energia potencjalna może zostać przekształcona w energię kinetyczną przy zachowaniu całkowitej energii układu, energia wewnętrzna układu termodynamicznego może zostać przekształcona w energię kinetyczną lub potencjalną. Podobnie jak potencjalenergia, energia wewnętrzna może być przechowywana w systemie.Zauważ jednak, że ciepło iprace nie mogą być przechowywane lub konserwowane niezależnie, ponieważ zależą one od procesu., Pierwsze prawo termodynamiki pozwala na istnienie wielu stanów systemu, ale tylko niektóre stany mogą istnieć w przyrodzie. Drugie prawo termodynamiki pomaga wyjaśnić tę obserwację.
Jeżeli układ jest w pełni izolowany od otoczenia zewnętrznego, możliwe jest wystąpienie zmiany stanu, wktórym do systemu nie jest przenoszone żadne ciepło. Naukowcy odnoszą się do procesu, który nie obejmuje heattransfer jako proces adiabatyczny.,Implementacja pierwszego prawa termodynamiki dla gazów wprowadza innycałkowita zmienna stanu zwana entalpią, która jest opisana na osobnej stronie.
zajęcia:
wycieczki z przewodnikiem
-
 Termodynamika:
Termodynamika: 
Nawigacja ..
![]()
![]()
![]()
Strona główna poradnika dla początkujących