Termodynamiikka on haara physicswhich käsittelee energiaa ja työtä järjestelmän.Thermodynamics käsittelee vain thelarge scale responseof järjestelmän, jonka voimme havainnoida ja mitata kokeissa. Pienimuotoiset kaasuvuorovaikutukset perustuvat kaasujen kineettiseen teoriaan.Termodynamiikan principallaweja on kolme, jotka kuvataan erillisillä dioilla., Eachlaw johtaa määritelmä ofthermodynamic ominaisuudetjotka auttaa meitä ymmärtämään ja ennustamaan toimintaa physicalsystem. Esittelemme joitakin yksinkertaisia esimerkkejä näiden lakien andproperties erilaisia fyysisiä järjestelmiä, althoughwe ovat kiinnostuneita termodynamiikan ofpropulsion systemsandhigh nopeus virtaa.Onneksi monet theklassiset esimerkit termodynamiikasta liittyvät kaasudynamiikkaan.,
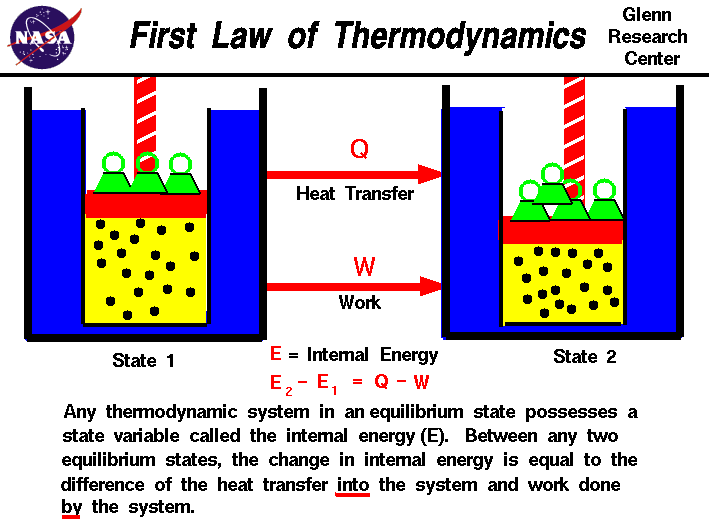
– meidän havaintoja työstä,tai kaasu, olemme havainneet, että työn määrä ei riipu onlyon alkuperäisen ja lopullisen valtioiden gasbut myös prosessi, tai polku, joka tuottaa lopullinen tila.Samoin kaasuun tai kaasusta siirretyn lämmön määrä riippuu myös alku-ja lopputiloista ja prosessista, joka tuottaa lopullisen tilan., Monet havainnot realgases ovat osoittaneet, että ero lämpö virtaa gasand työn kaasun riippuu vain alku-ja finalstates kaasun ja ei riipu prosessin tai pathwhich tuottaa lopullinen tila. Tämä viittaa siihen, olemassaolon anadditional muuttuja, jota kutsutaan sisäinen energia kaasu,joka riippuu vain valtion kaasun ja ei ole mitään prosessia.Sisäinen energia on tilamuuttuja, kuten lämpötila tai paine., Termodynamiikan ensimmäinen laki määrittelee internalenergy (E) on yhtä suuri ero lämmönsiirron (K) tulee järjestelmän ja työ (W) tehdä järjestelmässä.
E2 – E1 = Q – W,
– Olemme korostaneet thewords ”osaksi” ja ”by” in määritelmä. Lämpö poistetaan järjestelmästäwould be assigned a negative Signin in the equation. Samoin järjestelmän työlle annetaan negatiivinen merkki.,
sisäinen energia on vain energian muoto, kuten potentialenergy esine jossain korkeus maan yläpuolella, tai kineticenergy objektin liikkeessä. Samalla tavalla, että mahdolliset energycan voi muuntaa kineettistä energiaa säilyttäen yhteensä energyof järjestelmä, sisäinen energia ja termodynaaminen järjestelmä voi beconverted joko liike-tai potentiaalienergiaa. Kuten potentiaalinen energia, sisäinen energia voidaan varastoida järjestelmään.Huomaa kuitenkin, että lämpö andwork ei voida varastoida tai säilyttää itsenäisesti, koska ne arvioinnin prosessi., Termodynamiikan ensimmäinen laki mahdollistaa järjestelmän manypositiivisten tilojen olemassaolon, mutta vain tietyt valtiot ovat olemassa luonnossa. Termodynamiikan toinen laki auttaa tämän havainnon tekemisessä.
Jos järjestelmä on täysin eristetty ulkopuolelta ympäristö, se on osoittanut muuttaa tilaan, jossa ei lämpö siirretään osaksi järjestelmää. Tutkijat viittaavat prosessiin, jossa heattransfer ei ole adiabaattinen prosessi.,Täytäntöönpanon ensimmäinen laki termodynamiikan, kaasujen esittelee anotheruseful valtion muuttuja nimeltään enthalpywhich on kuvattu erillisellä sivulla.
Toiminnot:
opastukset
-
 Termodynamiikka:
Termodynamiikka: 
– Navigointi ..
![]()
![]()
![]()
Aloittelijan Opas Etusivu