Introducere
sindromul ovarului polichistic (PCOS) este una dintre cele mai frecvente tulburări ale endocrinologiei la femeile de vârstă reproductivă. PCOS este diagnosticat prin confirmarea prezenței a două dintre următoarele: oligo – și/sau anovulație, hiperandrogenism clinic și / sau biochimic și caracteristici ultrasunete ale ovarelor polichistice, cu excluderea altor etiologii (Fr și Tarlatzis, 2004)., Ratele de prevalență ale PCOS depind de criteriile de diagnostic utilizate, dar pot fi de până la 18% atunci când se utilizează criteriile de diagnostic Rotterdam (Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group, 2004). Hiperandrogenismul se găsește la 60-80% dintre femeile cu PCOS (Azziz et al., 2006). Clinice majore sau caracteristici biochimice de hiperandrogenism sunt acnee, hirsutism, alopecie, și dermatita seboreica; crescute de testosteron, androstendion, și dehidroepiandrosteron sulfat de niveluri; și a scăzut sex hormone binding globuline (SHBG) niveluri., Sindromul nu numai că prezintă manifestări reproductive, dar are și implicații metabolice, inclusiv rezistența la insulină, dislipidemia, obezitatea, diabetul de tip 2 și inflamația sistemică (Deugarte et al., 2005; Sartor și Dickey, 2005; Escobar-Morreale și colab., 2011).în timp ce tratamentul de primă linie pentru inducerea ovulației la femeile cu PCOS este administrarea de citrat de clomifen, se consideră că efectele antiestrogenice ale citratului de clomifen asupra endometrului și mucusului cervical determină o rată scăzută de concepție de 20% (Gonen și Casper, 1990)., Clomifenul citrat este, de asemenea, asociat cu o serie de efecte secundare, inclusiv bufeuri, disconfort mamar, distensie abdominală, greață, vărsături, nervozitate, cefalee, căderea părului și tulburări de vedere (Legro et al., 2007a). Studii recente au investigat rolul metforminei ca agent de sensibilizare la insulină și, deși utilizarea sa este în creștere, înțelegerea mecanismului său este incompletă (Legro et al., 2007b)., Mai mult, poate provoca dezvoltarea de foliculi multipli, împreună cu un risc de hiperstimulare ovariană, sarcini multiple și malformații congenitale, cum ar fi defecte de tub neural, ducând astfel la rezultate potențial nesatisfăcătoare ale tratamentului.deoarece PCOS este definit ca o tulburare metabolico-endocrină multifactorială (Laven et al., 2002), stilul de viață și dieta, în special dieta mediteraneană, joacă un rol relevant, alături de tratamentul farmacologic (Barrea et al., 2019)., Studii recente au sugerat că tratamentele complementare și alternative, inclusiv medicamentele pe bază de plante și acupunctura, pot atenua simptomele PCOS, dar dovezile eficacității și siguranței lor sunt insuficiente. Prin urmare, trebuie investigate noi strategii de tratament care încorporează terapii complementare și alternative pentru a optimiza tratamentul PCOS. În acest studiu, am analizat datele privind efectele și mecanismele care stau la baza medicamentelor pe bază de plante utilizate în tratamentul modelului PCOS în studiile de laborator.,
metode
articolele publicate în limba engleză până la 30 iunie 2018 au fost căutate în Medline (prin PubMed) și EMBASE (prin Elsevier). Termenii de căutare au fost o combinație de termeni medicali (MeSH) și sinonimele lor. Termenii de căutare Utilizați au fost după cum urmează: și .
criteriile de includere ale recenziei noastre au inclus următoarele:
1. Studii in vitro și in vivo care au evaluat efectele potențiale ale medicamentelor pe bază de plante asupra modelului PCOS
2., Cercetări asupra compușilor izolați din ierburi, extracte individuale din plante sau decocții pe bază de plante
3. Criteriile de excludere au fost următoarele:
1. Studii clinice cu medicamente pe bază de plante pentru PCOS
2. Articole de revizuire
3., Articole care nu descriu componentele medicamentului pe bază de plante; cu toate acestea, acest lucru a fost permis în cazul medicamentelor pe bază de plante brevetate
printre studiile preluate, după eliminarea duplicatelor, titlurile și rezumatele au fost revizuite pentru a găsi articole potențial relevante. Apoi, textele integrale ale articolelor analizate au fost revizuite pentru a confirma că au îndeplinit criteriile noastre de includere.,am extras date privind intervenția pe bază de plante; utilizarea celulelor țintă (sau a modelului animal); metoda de extracție pe bază de plante: calea de administrare; doza și perioadele; și rezultatele compușilor izolați din ierburi, extracte individuale din plante și decocții pe bază de plante. Pe baza acestor date, am rezumat acțiunile și mecanismele care stau la baza efectelor benefice ale medicamentelor pe bază de plante asupra modelului PCOS.
rezultate
caracteristicile studiului
în prezenta revizuire, am inclus un total de 27 de studii care au implicat 22 de medicamente pe bază de plante care au raportat eficacitatea lor pe modelul PCOS., Am identificat două studii in vitro, 22 de studii in vivo și trei studii cu experimente in vitro și in vivo. Intervențiile pe bază de plante din cele 27 de studii au cuprins patru compuși izolați din plante medicinale (6 studii), nouă extracte individuale din plante (11 studii) și nouă decocții pe bază de plante (10 studii). O diagramă a procesului de selectare a articolului este prezentată în Figura 1.
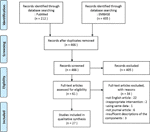
Figura 1 Diagrama de flux a procesului de selecție a studiului.,
Plante de Intervenții și de Laborator Rezultate
Compuși Izolați Din Plante
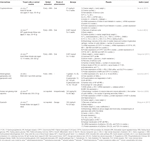
Tabelul 1 In vitro și in vivo de compuși izolați din plante (n=6).
extracte individuale din plante
Aloe vera (L.) Burm.f. niveluri plasmatice reduse ale colesterolului total (TC), trigliceridelor (TG) și colesterolului lipoproteinelor cu densitate scăzută (LDL-C); niveluri îmbunătățite ale colesterolului lipoproteinelor cu densitate mare (HDL-C) (Desai și colab.,, 2012); creșterea foliculară normalizată; și a recuperat ciclul estral (Maharjan și colab., 2010). Atractylodes macrocephala Koidz. a indus recuperarea ciclului estral și reducerea nivelului de testosteron, a nivelurilor de androstendionă, a indicelui de androgen liber, a nivelurilor de LH, a raportului LH/FSH și a nivelurilor hormonale anti-Mülleriene (Zhou et al., 2016). Matricaria chamomilla L.-tratat de sex feminin șobolani Wistar au arătat scăderea chisturi in tesutul ovarian și un număr crescut de foliculi dominante (Zangeneh et al., 2010). Cocos nucifera L., recuperat ciclul estral; TC redus, colesterol cu densitate foarte scăzută și niveluri de TG; și niveluri crescute de HDL-C (Soumya et al., 2014). Linum usitatissimum L.-tratat de sex feminin SD șobolani au arătat crescut de foliculi antral și corpus luteum, un număr scăzut de chistică a foliculilor, și cu diametru redus de foliculi antral (Jelodar et al., 2018). Foeniculum vulgare Mill. glomerul normal indus, membrana normală a subsolului și capilarele (Sadrefozalayi și Farokhi, 2014)., Zingiber officinale Roscoe a redus nivelurile de LH și estrogen și a crescut nivelurile de FSH și progesteron la șobolanii SD de sex feminin neonatal (Atashpour et al., 2017). Coreeană ginseng roșu (Panax ginseng C. A. Mey.)- șobolanii de sex feminin tratați cu SD au prezentat mai puțini foliculi chistici și expresia ARNm a NGF în ovare (Pak et al., 2009; Jung și colab., 2011). Labisia pumila var. alata a crescut viteza de perfuzare a glucozei și a redus nivelurile de TC și TG (Mannerås et al., 2010). Datele sunt rezumate în tabelul 2.,
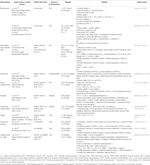
Table 2 In vitro and in vivo studies of individual herbal extracts (n=11).
Herbal Formula Decoctions
Bushen Tongmai recipe (composed of Astragalus membranaceus Bge, Radix Polygoni Multiflori, Herba Cistanches, Radix Salviae Miltiorrhizae, Radix Notoginseng, Radix Puerariae, Herba Epimedii, Rhizoma Chuanxiong, and Radix Rehmanniae) reduced serum fasting insulin and enhanced protein expression of Protein kinase Bα in thecal and granulosa cells of antral follicles (Li et al., 2010)., SD rats treated with Changbudodam-Tang (Rhizoma atractylodis, Rhizoma cyperi, Fructus ponciri, Pericarpium citri nobilis, Poria, Arisaematis Rhizoma, Radix glycyrrhizae, Massa Medicata Fermentata, and Zingiberis Rhizoma) and Yongdamsagan-Tang (Radix gentianae, Bupleuri Radix, Alimatis Rhizoma, Lignum akebiae, Plantaginis Semen, Hoelen, Rehmanniae Radix, Angelicae Gigantis Radix, Gardeniae Fructus, Scutellariae Radix, and Radix glycyrrhizae) showed a reduced number of cystic follicles, a higher number of growing secondary follicles, and reduced expression of NGF in ovaries (Lee et al., 2003)., Medicina naturista chineza (CHM) 1 (Rădăcină de Astragali Rădăcină de Rehmanniae Preparata, Cuscuta mine din china Lam, Fructe Viața Lucidi, Fructe Psoraleae, Radacina de Salviae Miltiorrhizae, și zmeura Linn) și CHM 2 (Cuscuta mine din china Lam, Fructe Viața Lucidi, și zmeura Linn) induse de recuperare a ciclului estral și LH/FSH raport, și reducerea de androstendion ar trebui să nivelurile și androgeni liberi index (Gu et al., 2015)., Gui Zhu Yi Kun formula (GZYKF) (Semen Cuscutae, Rhizoma Atractylodis Macrocephalae, Angelica sinensis, Adenophora tetraphylla, Plantago asiatica, Rubia cordifolia, și Luffa cilindrica) a redus arnm expresii de Beclin 1, lumina lanț 3, și supresoare tumorale p53 (Xing et al., 2017). HemoHIM (Angelica Radix, Cnidii Rhizoma, și Paeonia Radix)-tratat SD femelele de șobolan au arătat crescut ca număr și dimensiune a corpilor luteali și un nivel scăzut de NGF proteine în ovare (Kim et al., 2009). Sa constatat că Heqi san reduce nivelul de LH și testosteron și atenuează rezistența la insulină (Zhao et al., 2017)., Un roman pe bază de plante medicament imunomodulator (IMOD) (Rosa canina, Urtica dioica, și Tanacetum vulgare)-tratat de sex feminin albino șobolani Wistar-a arătat mai puține cazuri de ovariene închid complet și chistică a foliculilor, și un număr mai mare de corpora lutea (Rezvanfar et al., 2012). Kyung-Ok-Ko (KOK) administrarea induse de recuperare a ciclului estral și cluster de diferențiere (CD)11b, CD3, IL-1β, IL-6, TNF-α, IL-8, monocite chemoatractant protein (MCP)-1, și iNOS arnm expresie reducere în ovare la femele de șobolani SD (Jang et al., 2014; Lee și colab., 2016)., De sex feminin SD șobolanii tratați cu Xiao Yao San (XYS) (radix bupleuri, angelica, radix paeoniae alba, rhizoma atractylodis macrocephalae, poria, ghimbir, menta, și glycyrrhizae) au arătat un număr redus de chistică a foliculilor și a redus terminal deoxynucleotidyl transferaza dUTP nick end etichetare (TUNEL) celule pozitive în foliculi antral (Sun et al., 2017). Datele sunt rezumate în tabelul 3.

Masa 3 In vitro și in vivo de formulă pe bază de plante decocturi (n=10).,
acțiunile medicamentelor pe bază de plante pentru tratarea PCOS

Tabelul 4 acțiunile medicamentelor pe bază de plante pentru tratarea PCOS.
mecanismele de acțiune pentru PCOS

Tabelul 5 mecanismele de acțiune ale medicamentelor pe bază de plante pe PCOS.,analiza noastră a literaturii publicate până la 30 iunie 2018 a rezumat constatările studiilor in vitro și in vivo privind eficacitatea medicamentelor pe bază de plante pentru tratamentul modelului PCOS. Un total de patru compuși izolați din ierburi (6 studii), nouă extracte individuale din plante (11 studii) și nouă decocții pe bază de plante (10 studii) au fost găsite pentru a avea efecte inhibitoare asupra PCOS., Conform rezultatelor raportate, medicamentele pe bază de plante au normalizat hormonii feminini, au diminuat hormonii masculini, au recuperat ciclul estral, au ameliorat rezistența la insulină și au îmbunătățit metabolismul lipidic. Am constatat că activitatea potențială inhibitoare a medicamentelor pe bază de plante ar putea influența diferite aspecte ale PCOS, cu efectele benefice ale medicamentelor pe bază de plante care apar în principal prin anti-inflamație, stres anti-oxidativ, inhibarea autofagiei sau apoptozei și reducerea NGF ovarian.,
medicamentele pe bază de plante pot inhiba afecțiunile inflamatorii ale PCOS
studii recente au explorat în continuare etiologia și patologia PCOS. Oamenii de știință au descoperit că în micromediul pacienților cu PCOS, inflamația cronică ușoară este un semn distinctiv al sindromului (Nestler, 2000). PCOS a fost relevant În inflamația cronică (Benson et al., 2008), iar macrofagele au fost patogeneza sa majoră (Wu et al., 2004). Macrofagele ovariene produc citokine, chemokine și factori de creștere atât în procesele normale, cât și în cele inflamatorii ale ovarului., Macrofagele pot Orchestra apoptoza și remodelarea țesuturilor, care sunt implicate în foliculogeneză, ovulație și formarea corpului luteal (Benson et al., 2008). Având în vedere rolul critic al macrofagelor în PCOS (Benson et al., 2008), numeroase studii au comparat nivelurile de citokine în ser și în fluidele foliculare la pacienții cu PCOS. Valorile TNF-α și IL-6 în ser și în fluidele foliculare au fost crescute la pacienții cu PCOS non-obezi/non-diabetici tratați cu gonadotrofine (Amato et al., 2003)., Proteinele inflamatorii macrofage-1α și MCP-1 au fost crescute la pacienții cu PCOS și asociate cu adipozitatea (Glintborg et al., 2009). iNOS, ciclooxigenaza-2 (COX-2) și activitatea factorului de creștere transformant (TGF) – β au fost crescute în ovarele pacienților cu PCOS (Elia et al., 2006; Hatzirodos și colab., 2011), iar activitatea inos și COX-2 au fost prevenite prin administrarea metforminei (Elia et al., 2006). Aceste rezultate sugerează că sistemul imunitar este relevant pentru patogeneza PCOS., Prin urmare, noi remedii care vizează acest proces inflamator pot fi o alternativă terapeutică la tratamentul actual.în această revizuire, iridoizii au inhibat semnificativ expresia IL-1β, IL-6, IL-10 și inos, inhibând astfel condițiile inflamatorii (Zuo et al., 2017). De asemenea, quercetinul a redus semnificativ nivelurile de IL-1β, IL-6 și TNF-α și a scăzut translocarea nucleară a factorului nuclear kappa B (NF-kB) într-un model de șobolan PCOS rezistent la insulină (Wang et al., 2017)., Pre-administrarea KOK a diminuat expresia crescută a moleculei adaptorului de legare a calciului ionizat -1 ( + ) macrofage în stratul celular tecal al chisturilor și stroma. KOK a crescut, de asemenea, expresia ARNm a CD11b și CD3 în țesutul ovarian PCOS. Preadministrarea KOK a scăzut semnificativ nivelurile crescute de IL-1β, IL-6, IL-8, TNF-α, MCP-1 și inos; și a crescut expresia redusă a ARNm a factorului de creștere epidermal și a TGF-β în ovarele PCOS., Aceste rezultate au demonstrat că Kok reglează expresia mediatorilor inflamatori în modelul PCOS indus de dehidroepiandrosteron (DHEA) (Jang et al., 2014). Mediatorii inflamatori au fost, de asemenea, reglementați în endometrul uterului prin administrarea KOK, care sa dovedit a preveni hiperplazia endometrială la modelele PCOS (Lee et al., 2016). De asemenea, sa demonstrat că TNF-α în ser și prostaglandina E (PGE) în ovar au fost scăzute de IMODs (Rezvanfar et al., 2012).,
Medicamente pe bază de Plante Pot Atenua Stresul Oxidativ în acest SINDROM
de specii Reactive de oxigen sunt molecule semnal important în reglarea unor functii fiziologice in reproducere feminin, inclusiv steroidogeneza, foliculogeneza, maturarea ovocitului, corpus luteum funcție, și luteolysis (Agarwal și colab., 2005). În plus, ele joacă un rol-cheie în procesele patologice ale reproducerii feminine (Agarwal et al., 2003; Agarwal și colab., 2008)., Stresul oxidativ este o afecțiune în care echilibrul dintre capacitatea antioxidantă a organismului și produsele toxice derivate din oxigen și/sau azot este afectat. În consecință, radicalii liberi sunt insuficient detoxificați de antioxidanții celulari. Stresul oxidativ joacă un rol important în reproducerea feminină (Ruder et al., 2008; Ruder și colab., 2009; Vakilian și colab., 2009) și există o literatură din ce în ce mai mare cu privire la efectele markerilor de stres oxidativ crescut la femeile infertile și la implicarea lor în fiziopatologia PCOS (Joo et al., 2010; Mohamadin și colab., 2010)., PCOS se caracterizează prin inflamație cronică, stres oxidativ și expresie microRNA anormală (Zhao et al., 2015; Zuo și colab., 2016). Deoarece se știe că inflamația și stresul oxidativ sunt strâns legate, stresul oxidativ crescut rezultă de obicei din și duce la o afecțiune inflamatorie (Zuo et al., 2016). Este dificil să se separe inflamație de stresul oxidativ, și s-a propus în ultimii ani că inflamația și stresul oxidativ cuprinde fundamentul principal de apariție a bolii (Duleba și Dokras, 2012).în această recenzie, IMODs( Rezvanfar et al.,, 2012) și iridoizi (Zuo et al., 2017) a arătat efecte pozitive asupra stresului oxidativ/nitrosativ, direct sau indirect, în principal prin reducerea radicalilor liberi și inhibarea citokinelor inflamatorii la șobolanii PCOS. Administrarea IMODs a redus semnificativ peroxidarea lipidică (un marker al stresului oxidativ) și a crescut nivelurile de superoxid dismutază, catalază și glutation peroxidază (markeri ai potențialului antioxidant) în PCOS indus de hiperandrogenism. În plus, peroxinitritul (un marker al stresului nitrosativ), TNF-α și nivelurile PGE au fost reduse semnificativ de IMODs., În plus, aceste efecte de IMODs au fost în concordanță cu dovezi histologice, care au arătat o îmbunătățire semnificativă a caracteristicilor microscopice de foliculogeneza în comparație cu cei din grupul de control (Rezvanfar et al., 2012). Sistemul de semnalizare NF-kB este cunoscut ca o paradigmă dominantă pentru moleculele specifice de transducție a semnalului, activarea genelor și proteinele reglatoare ca răspuns la inflamație (Ivanenkov et al., 2011)., De iridoide eficient atenuat lipopolysaccharide induse de altitudine de IkB fosforilarea niveluri, a scăzut IkB nivel de expresie, și a scăzut NF-kB P65, indicând faptul că iridoide exercita efectele lor antioxidante, prin intermediul NF-kB cale (Zuo et al., 2017).
medicamentele pe bază de plante pot regla apoptoza și/sau Autofagia în PCOS
supraviețuirea sau moartea celulelor granuloase este recunoscută ca un factor critic care afectează soarta foliculilor (Matsuda et al., 2012). Apoptoza și autofagia sunt două forme de moarte celulară programată., Autofagia este procesul prin care un autofagozom, care este o veziculă cu membrană dublă, transportă Material citoplasmatic la lizozom (Mizushima și Komatsu, 2011). S-a raportat că atât apoptoza, cât și autofagia pot fi induse în celulele granuloase și că acestea sunt implicate în controlul dezvoltării foliculare (Choi et al., 2010; Choi și colab., 2013). Celulele granuloase sunt recunoscute ca jucători critici în dezvoltarea foliculilor. Ele produc estradiol, factori de creștere asemănătoare insulinei și alte citokine în ovar și exprimă receptorii pentru estradiol, LH și FSH (Juengel et al.,, 2006), toate acestea participă la reglementarea dezvoltării foliculilor. Astfel, orice afectare a celulelor granuloase poate duce la dezvoltarea dezordonată a foliculilor.în ultimul deceniu, au fost identificate căile de semnalizare legate de autofagie și regulatorii lor majori de proteine. Proteina asociată microtubulului de șobolan 1 lanț ușor 3 este asociată cu procesarea membranei autofagozomilor (Kabeya et al., 2000). Beclin-1 a fost, de asemenea, demonstrat că are un rol critic în formarea autofagozomilor (Von Hoven et al., 2012)., Mai mult, studiile anterioare au identificat supresorul tumoral p53 (p53) ca modulator dual al autofagiei în reglarea morții celulare sau a supraviețuirii (Vouden și Ryan, 2009; Zhang et al., 2010). La niveluri scăzute de energie, protein kinaza activată de adenozin monofosfat (AMPK), care este activată de p53, este capabilă să activeze complexul sclerozei tuberoase 2 și, prin urmare, să inhibe ținta mamiferă a activității rapamicinei (mTOR) și să crească autofagia (Feng et al., 2007)., În acest review, p53, care este activat prin GZYKF în nucleu, la rândul său activat AMPK și sestrin, care acționează ca un feedback în mTOR inhibiție, activând astfel autofagie. Autofagia este, de asemenea, modulată de căile de semnalizare a fosfoinozitidei 3-kinazei/protein kinazei B (PI3K/Akt) (Pyo et al., 2012). În acest review, XYS atenuat reducerea fosforilării proteinei ribozomale S6 kinaza polipeptidice am și Akt, precum și creșterea de microtubuli-proteine asociate lumina lanț 3-am să microtubuli-proteine asociate lumina lanț 3-II de conversie atât in vivo cât și in vitro (Sun et al., 2017).,endometria la majoritatea pacienților cu PCOS este groasă și prezintă hiperplazie simplă, complicată sau atipică sau transformare malignă care poate fi corelată cu apoptoza celulelor endometriale (Villavicencio et al., 2007). Hiperandrogenism induse de DHEA este asociat cu un număr mai mare de celule apoptotice în endometria, și metformină (un insulinomimetic sau insulino-sensibilizant, agent) este capabil de a reduce numărul crescut de celule apoptotice (Elia et al., 2009). În această revizuire, moartea celulelor apoptotice a fost evaluată prin colorarea tunelului., Celulele apoptotice au fost rareori detectate prin colorarea tunelului în țesutul uterin al grupului fals sau al grupului KOK. Cu toate acestea, numărul de celule TUNEL-pozitive a fost crescut în endometria grupului DHEA. Numărul crescut de celule apoptotice a fost redus semnificativ după administrarea KOK. Aceste rezultate indică faptul că administrarea prealabilă a KOK a inhibat malformația endometrială indusă de DHEA prin reducerea apoptozei endometriale (Lee et al., 2016).,studiile anterioare au arătat că PCOS este asociat cu activarea anormală a sistemului nervos simpatic, ducând la creșterea nervilor catecolaminergici (Semenova, 1969), metabolismul norepinefrinei afectat (Garcia-Rudaz et al., 1998) și creșterea activității nervilor simpatici prin nervul ovarian superior (Lara et al., 1993)., Dezvoltarea și funcția inervației simpatice ovariene depind de ovar pentru producerea NGF, un neurotrofin derivat din țintă necesar pentru dezvoltarea sistemului simpatic periferic (Levi-Montalcini, 1987). Familia neurotrofină implică receptorul NGF și ARNm NGF în ovulație și în fiziopatologia PCOS (Lara et al., 2000; Stener-Victorin și colab., 2003). În ovarele de șobolan, NGF este sintetizat în principal în celulele peretelui folicular (Dissen et al.,, 1996), iar în PCOS, activarea NGF poate fi un factor implicat în creșterea fluxului de norepinefrină către glandă, care este indusă de valeratul de estradiol (EV) (Lara et al., 2000) PCOS prezintă o densitate ridicată a fibrelor nervoase intraovariene care este asociată cu hiperresponsivitatea simpatică (Stener-Victorin et al., 2003).
În această revizuire, administrarea de formule pe bază de plante Changbudodam-Tang și Yongdamsagan-Tang scăzut semnificativ crescute NGF în ovare cu prea puțin efect asupra tesutului creierului (Lee et al., 2003)., HemoHIM a normalizat, de asemenea, NGF, a redus numărul mare de foliculi antrali și a crescut numărul de corpus lutea în PCOS. Aceste rezultate sunt în concordanță cu cele ale studiilor anterioare privind efectele benefice ale HemoHIM în prevenirea și tratamentul PCOS (Pak et al., 2009). În plus, administrarea extractului de ginseng roșu coreean (Pak et al., 2009; Jung și colab., 2011) și saponine totale de ginseng roșu coreean (Pak și colab., 2005) a scăzut semnificativ expresia proteinei NGF și a ARNm NGF, comparativ cu cele din ovarele tratate cu EV.,acest studiu a revizuit dovezile pentru medicamentele pe bază de plante care pot fi utilizate pentru a trata PCOS și simptomele asociate, iar constatările sunt destinate să adauge la înțelegerea clinicienilor a mecanismelor de acțiune ale medicamentelor pe bază de plante în tratamentul PCOS. Principala limitare a studiului nostru este eterogenitatea intervențiilor. În plus, studiul nostru nu a efectuat o evaluare a calității fiecărui studiu sau o sinteză cantitativă a rezultatelor. Sunt justificate studii suplimentare care includ evaluarea metodologică a calității și sinteza cantitativă a rezultatelor.,în această revizuire, Un total de 27 de studii care au implicat 22 de medicamente pe bază de plante au prezentat efecte benefice asupra PCOS. Intervențiile pe bază de plante din cele 27 de studii au cuprins patru compuși izolați din plante medicinale (6 studii), nouă extracte individuale din plante (11 studii) și nouă decocții pe bază de plante (10 studii). Medicamentele pe bază de plante s-au dovedit a normaliza hormonii feminini, a diminua hormonii masculini, a recupera ciclul estral, a ameliora rezistența la insulină și a îmbunătăți metabolismul lipidic în PCOS., Mecanismele care stau la baza efectelor benefice ale medicamentelor pe bază de plante asupra PCOS sunt asociate cu anti-inflamație, stres anti-oxidativ, inhibarea autofagiei și/sau apoptozei și reducerea NGF ovarian. Medicamentele pe bază de plante pot fi considerate resurse promițătoare în dezvoltarea agenților terapeutici eficienți pentru PCOS.
contribuțiile autorului
I-HC și KP au proiectat studiul. C-YK și KP au căutat articolele și au analizat datele. KP a scris manuscrisul și I-HC L-a revizuit. Toți autorii au contribuit la articol și au aprobat versiunea trimisă.,
finanțare
această lucrare a fost susținută de Fundația Națională de cercetare din Coreea (NRF) grant finanțat de Guvernul Coreei (MSIP) (nr.NRF-2017r1c1b1006387) și societatea coreeană de Ginseng (2019).
Conflict de interese
autorii declară că cercetarea a fost efectuată în absența oricăror relații comerciale sau financiare care ar putea fi interpretate ca un potențial conflict de interese.,terol; LH, Luteinising hormone; MCP, monocyte chemoattractant protein; MeSH, medical subject heading; mTOR, inhibit mammalian target of rapamycin; NF-κb, nuclear factor kappa B; NGF, nerve growth factor; p53, tumor suppressor p53; PCOS, polycystic ovary syndrome; PGE, prostaglandin E; PI3K, phosphoinositide3-kinase; SD, Sprague Dawley; SHBG, sex hormone binding globulin; TC, Total cholesterol; TG, Triglyceride; TGF, transforming growth factor; TNF, tumor necrosis factor; TUNEL, terminal deoxynucleotidyl transferase dUTP nick end labeling; VLDL-C, Very low density cholesterol; XYS, Xiao-Yao-San.,
Rotterdam ESHRE / ASRM-Sponsored PCOS Consensus Workshop Group (2004). Revizuit consensul din 2003 privind criteriile de diagnostic și riscurile de sănătate pe termen lung legate de sindromul ovarului polichistic. Sterilitatea Fertilității 81 (1), 19-25. doi: 10.1016 / j. fertnstert.2003.10.004
CrossRef Textul Complet | Google Scholar
Semenova, I. (1969). Inervația adrenergică a ovarelor în sindromul Stein-Leventhal. Vestnik Akademii Meditsinskikh Nauk SSSR 24 (9), 58.
Google Scholar