En acetal er en funksjonell gruppe med tilkobling R2C(ELLER’)2). Her, R-grupper kan være økologisk fragmenter (et karbonatom, med vilkårlig andre atomer knyttet til det) eller hydrogen, mens R’ gruppene skal være økologisk fragmenter ikke hydrogen. De to R’ grupper kan være ekvivalent til hverandre (en «symmetrisk acetal») eller ikke (en «blandet acetal»)., Acetals er dannet fra og omgjøres til aldehyder eller ketoner og har samme oksidering staten ved sentral karbon, men har vesentlig forskjellige kjemiske stabilitet og reaktivitet forhold til det analoge karbonyl forbindelser. Den sentrale karbonatom har fire obligasjoner til det, og det er derfor mettet og har tetrahedral geometri.,

Generell struktur av acetals
begrepet ketal er noen ganger brukt til å identifisere strukturer assosiert med ketoner (både R-grupper organisk fragmenter snarere enn hydrogen) snarere enn aldehyder og historisk begrepet acetal ble brukt spesielt for aldehyd-relaterte saker (etter å ha minst ett hydrogen i stedet for en R på sentrale karbon). Den IUPAC opprinnelig fraråder bruken av ordet ketal helt, men har siden snudd sin avgjørelse., Imidlertid, i motsetning til historisk bruk, ketals er nå et delsett av acetals, et begrep som omfatter nå både aldehyd – og keton-avledet strukturer.
Hvis en av R-gruppene har en oksygen som den første atom (som er, det er mer enn to oxygens enkelt-bundet til den sentrale karbon), den funksjonelle gruppen er i stedet en orthoester. I motsetning til varianter av R, både R’ grupper er organisk fragmenter. Hvis en R’ er en hydrogen, den funksjonelle gruppen er i stedet en hemiacetal, mens hvis begge deler er H, den funksjonelle gruppen er et keton hydrat aldehyd eller fuktighet.,
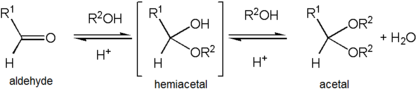
Dannelse av en acetal oppstår når hydroksyl gruppe av en hemiacetal blir protonated og er tapt vann. Den carbocation som er produsert så raskt angrepet av et molekyl av alkohol. Tap av proton fra festet alkohol gir acetal.,
Acetals are stable compared to hemiacetals but their formation is a reversible equilibrium as with esters., Som en reaksjon for å skape en acetal inntektene, vann må fjernes fra reaksjonsblandingen, for eksempel, med en Dean–Stark apparater, for at det hydrolyse av produktet tilbake til hemiacetal. Dannelsen av acetals reduserer det totale antall molekyler er tilstede (karbonyl + 2 alkohol → acetal + vann), og derfor er generelt ikke gunstig med hensyn til entropi. En situasjon der det ikke er entropically ugunstige er når en enkelt diol molekylet er brukt i stedet for to separate alkohol-molekyler (karbonyl + diol → acetal + vann)., En annen måte å unngå entropisk kostnaden er for å utføre syntese av acetal exchange, ved hjelp av en pre-eksisterende acetal-type reagens som-ELLER » – gruppe donor snarere enn enkle tillegg av alkohol i seg selv. En type reagens som brukes for denne metoden er en orthoester. I dette tilfellet, vann produsert sammen med acetal produktet blir ødelagt når det hydrolyses gjenværende orthoester molekyler, og denne siden reaksjonen produserer også mer alkohol for å bli brukt i de viktigste reaksjon.,
Acetals er brukt som beskytter grupper for karbonyl grupper i organisk syntese fordi de er stabile med hensyn til hydrolyse av baser og med hensyn til mange oksiderende og reduksjonsmidler. De kan enten beskytte karbonyl i et molekyl (ved midlertidig reagerer det med en alkohol) eller en diol (ved midlertidig reagerer det med en karbonyl). Som er, enten det karbonyl, eller alkohol, eller begge kan være en del av molekylet som reaksjon er å bli kontrollert.
Ulike spesifikke karbonyl forbindelser har spesielle navn for sine acetal former., For eksempel, en acetal dannet fra formaldehyd (to hydrogens knyttet til den sentrale karbon) er noen ganger kalt en formell eller methylenedioxy gruppe. Den acetal dannet fra aceton er noen ganger kalt en acetonide.