開発するスキル
- ラヴォアジエが”現代化学の父”と呼ばれる理由を理解する
- 精度と精度を区別する
ハリー-ポッターの魔法の薬醸造のような錬金術を化学の科学に変えたのは何が起こったのでしょうか? 測定しました。 量の注意深く、注意深い測定、固まりのような、容積、密度、温度、圧力。
測定の初期のヒーローはAntoine Lavoisierでした。, 彼は最初の真の化学科学者の一人でした。 真正面から向き合ってく実験のための描画な結論以外に必要とされるデータです。 彼は、事実、アイデア、言葉はできるだけ密接に関連しているべきだと言いました:あなたの思考を改善することなくあなたの言語を改善することは そこで彼は体系的な化学命名法を開拓しましたそれは本質的に私たちが今日使用しているものです。, 驚くべきことに、初心者に化学を導入することを意図した1789年に書かれた彼のテキストを読むと、その多くは現代の基準ではまだ完全に理解でき、
.jpg?revision=1&size=bestfit&width=200&height=272)
ラヴォアジエは、まず物質の状態を説明します:気体、液体、固体。 彼は、固体材料が加熱されると、膨張する傾向があり、最初は一定の体積を占める液体になるが、固体とは異なり注ぐことができると指摘している。, より多くの加熱、そしてそれは圧力に応じて異なるボリュームに拡大または圧縮されますので、彼は弾性として説明ガスになります。 ギリシャの哲学者とは異なり、彼はこれが物理的な変化であり、化学的変化ではないことを理解し、彼は何が起こっているかの良いサブミクロスケールの直観を持っています:材料の粒子は変化しない、彼らはさらに離れて取得します。,
彼は硫黄とリンと木炭(炭素)を燃やし、彼の本、図1からの図面に示すように、多くの場合、水銀のバケツの上に鐘の瓶を使用して、慎重に観察 これは、反応物化学物質が異なる生成化学物質に変わる化学変化または化学反応の例である。 あなたは空気の鐘の瓶の下にdとラベルされた皿に硫黄を点灯した場合、それはいくつかの余分な硫黄を残して出て行くまで、それは燃えます。 瓶の中に残っている空気は、もはや呼吸には適していません。 あなたが瓶にマウスを入れると、炎がしたのと同じように、それは死ぬでしょう。, これは、反応物を制限する概念を示しています。 反応または燃焼は酸素を使い果たしたときに停止し、主に窒素(およびいくつかの微量の他のガス)を瓶に残しました。 プリーストリー、別の科学者は、純粋な酸素ガスを調製する方法を彼に示し、彼は同様に多くの燃焼実験を行うためにこれを使用しました。
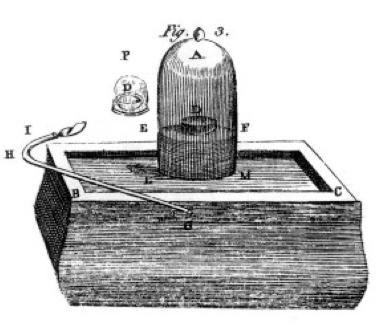
ラヴォアジエは測定に夢中でした。, 彼はすべてを測定する精巧な装置を開発しました。 図1に示すように、彼はリンを燃やし、白いフレーク状の製品の形成を観察します。 リン(この場合の反応物)は水溶性ではなかったが、生成物は水溶性であったので、彼は水で洗浄することによって未反応のリンから分離し、非常に慎重 乾燥後、彼はどのくらいのリンが燃えたか、どのくらいの酸素が消費されたか(酸素ガスの密度を知っていたため)、どのくらいの製品が形成されたかを測ることができた。, 彼は、生成物の質量は、すべての実験で消費された反応物の質量の合計であることを発見しました。 これは質量保存の法則です(実際には、以前の錬金術師や化学者も使用していました)。 彼はまた、リンには味がないことを観察しましたが、リン酸と呼ばれる製品は酸っぱいです。 彼はこれらの実験から、多くの場合、元素は特定の割合でのみ結合し、酸素は硫黄、リンなどと二つの異なる比率で結合できることを知っていました。, 彼は私たちが今日使用している用語を教えてくれました:硫酸は硫黄とより多くの酸素で構成され、亜硫酸は硫黄とより少ない酸素で構成されて -ouは酸素が少ないことを意味し、icは酸素が多いことを意味します。 詳細は命名法のページを参照してください。
ラヴォアジエは精度と精度に細心の注意を払いました。 たとえば、先ほど説明した実験では、反応の前後にベルジャー内のガスの量を測定しましたが、反応後は元の温度に戻るまで待たなければならないことに注意しました。, 反応後の体積を測定するときにガスが熱い場合、ガスは膨張しており、標準密度は適用されません。 実験を実行するたびに、実際よりも多くのガスが残っており、測定が正確ではないと考えるでしょう。 実験の平均結果が正しい値に近い場合、それは正確です。 ただし、平均が正しく、実験が正確であっても、実験が毎回非常に異なる数値を与える場合は、正確ではありません。, 精度は、”2時ごろ”と”3分27秒前”の2時間前のミーティングの違いです。”精度とは、あなたがどれだけ具体的で、どれだけ詳細を使用しているかです。 ラヴォアジエはまた、現在韓国や他の多くの国で使用されている単位(kg、L、m)のシステムの開発にも貢献しました。

全体的に、彼はこれまで誰もやっていなかった非常に多くのオリジナルの実験を行っていませんでしたが、彼は非常に慎重に実験を行ったので、できるだけ正確かつ正確であり、それから彼はそれらについて明確に考え、すべてを明確にするのに役立つ化学物質やアイデアを記述する言葉を作りました。, Lavoiserの前に書かれた化学の教科書を読むと、化学物質の名前は化学物質が何であるかに基づいているのではなく、歴史に基づいている(そしてハリー-ポッターから来たように聞こえる)ので、あなたは非常に混乱するでしょう。 Lavoiserの後に書かれた化学のテキストを読むと、今日の私たちが使用しているものと同様の言語が認識されます。
Summary
精度は、測定値が実際の値にどれだけ近いかを示します。 精度は、測定値のグループが互いにどれだけうまく一致するかを表します。, 質量保存法則は、物質は化学的または物理的なプロセスによって作成も破壊もできないと述べています。 これは、任意の実験で消費される反応物の質量の合計が生成物の質量に等しいことをもたらす。 化学的変化は、新しい物質が形成されるように物質の化学的同一性を変化させることを含む。 物理的な変更は化学アイデンティティを変えないで物質の変更を含む。 燃焼と錆は化学プロセスの二つの例であり、沸騰と溶融は物理プロセスの例である。, 化学反応は、反応物、化学変化の過程で消費される化学物質を、反応物とは異なる組成を有する化学変化の過程を通じて生成される化学物質に変えることを含む。 制限反応物質は、化学反応から生成され得る生成物の量を決定するか、または制限する。
外部リンク
- クラッシュコース化学:基本法則(11分)
貢献者と帰属
-
エミリー-V-イームズ(サンフランシスコ市立大学)