The chemical element hafnium is classed as a transition metal . It was discovered in 1923 by Georg von Hevesy and Dirk Coster.

Data Zone
| Classification: | Hafnium is a transition metal |
| Color: | silvery |
| Atomic weight: | 178.,49 |
| State: | solid |
| Melting point: | 2230 oC, 2503 K |
| Boiling point: | 4600 oC, 4873 K |
| Electrons: | 72 |
| Protons: | 72 |
| Neutrons in most abundant isotope: | 108 |
| Electron shells: | 2,8,18,32,10,2 |
| Electron configuration: | 4f14 5d2 6s2 |
| Density @ 20oC: | 13.,2 g/cm3 |
Show more, including: Heats, Energies, Oxidation,
Reactions, Compounds, Radii, Conductivities
| Atomic volume: | 13.6 cm3/mol |
| Structure: | hcp: hexagonal close pkd |
| Hardness: | 5.5 mohs |
| Specific heat capacity | 0.14 J g-1 K-1 |
| Heat of fusion | 27.2 kJ mol-1 |
| Heat of atomization | 621 kJ mol-1 |
| Heat of vaporization | 575.,0 kJ mol-1 |
| 1st ionization energy | 658.5 kJ mol-1 |
| 2nd ionization energy | 1440 kJ mol-1 |
| 3rd ionization energy | 2250 kJ mol-1 |
| Electron affinity | 178 kJ mol-1 |
| Minimum oxidation number | 0 |
| Min. common oxidation no. | 0 |
| Maximum oxidation number | 4 |
| Max. common oxidation no. | 4 |
| Electronegativity (Pauling Scale) | 1.,3 |
| Polarizability määrä | 16.,none |
| Oxide(s) | HfO2 |
| Hydride(s) | HfH2 |
| Chloride(s) | HfCl4 |
| Atomic radius | 155 pm |
| Ionic radius (1+ ion) | – |
| Ionic radius (2+ ion) | – |
| Ionic radius (3+ ion) | – |
| Ionic radius (1- ion) | – |
| Ionic radius (2- ion) | – |
| Ionic radius (3- ion) | – |
| Thermal conductivity | 23.,2 W m-1 K-1 |
| sähkönjohtavuus | 3,4 x 106 S m-1 |
| Jäätymispiste/Sulamispiste: | 2230 oC, 2503 K |

Hafnium metalli on hopea väri. Se näyttää normaalisti melko harmaalta ilmassa muodostuvan oksidikerroksen vuoksi. Hafnium-jauhe, ilman oksidikerrosta, voi syttyä itsestään ilmassa. Kuvan Viite., (1)
Löytö Hafnium
Hafnium olemassaolo oli alun perin ennustettu venäjän kemisti Dmitri Mendelejev. Hänen 1869 kirja ”Määräajoin Lakia alkuaineita”, hän ennusti olemassaolon elementin kanssa samanlaisia ominaisuuksia, mutta raskaampaa kuin titaani ja zirkonium.
vuonna 1911 harvinaisen maametallin lutetiumin löytäjä Georges Urbain luuli löytäneensä alkuaineen 72 harvinaisten maametallien spektrianalyysissä. Hän kutsui tätä uutta elementtiä celtium, mutta kolme vuotta myöhemmin se oli osoitettu olevan sekoitus jo löytäneet lantanidit., (2)
Vuonna 1921, Neils Bohr ehdotti unkarilainen kemisti Georg von Hevesy etsiä puuttuva elementti zirkonium malmit. (3) Bohrin atomirakenteen kvanttiteorian mukaan näillä metalleilla olisi samanlaisia kemiallisia ominaisuuksia, joten oli hyvä mahdollisuus, että ne löytyisivät samoista malmeista.
Seuraavat Bohr neuvoja, Hevesy ja hollantilainen fyysikko Dirk Coster löysi hafnium vuonna 1923 käyttäen x-ray spektroskopia analysoida zirkonium malmit.
Anton Eduard van Arkel ja Jan Hendrik de Boer löydettiin menetelmä tuottaa erittäin puhdasta hafnium vuonna 1925., Hafnium tetraiodide (HfI4) on hajonnut valkoinen kuuma volframi hehkulanka luoda crystal bar puhdas, hafnium. Tätä kutsutaan kristallipalkin prosessiksi.
– elementti oli nimeltään Hafnium jälkeen latinankielinen nimi ’Hafnia, eli Kööpenhaminan kaupunki, jossa tekijä löydettiin.

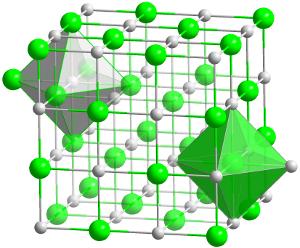
Crystal rakenne hafnium carbide (HfC)., Tämä on tulenkestävin (lämmönkestävä) yhdiste, joka tunnetaan kahdesta elementistä suhteessa 1: 1.

Hafnium on käytetty reaktorin säätösauvat sisään ydinsukellusveneiden

Valkoinen hafnium (IV) oksidi (HfO2). Hafniumoksidipohjaisia yhdisteitä tuodaan piipuihin tuottamaan pienempiä, suorituskykyisiä prosessoreita, joiden energiatehokkuus on parantunut.,
Ulkoasu ja Ominaisuudet
Haitallisia vaikutuksia:
Hafnium pidetään myrkyttömiä. Jauhemaisessa muodossa se on pyroforinen (voi syttyä itsestään).
Ominaisuudet:
Hafnium on kiiltävä, hopeanhohtoinen, sitkeää metallia.
kemiallisesti se muistuttaa zirkoniumia.
Kun läsnä yhdisteet hafnium on olemassa lähinnä hapettumista valtion IV.
Hafnium kestää korroosiota, koska muodostumista oksidikalvon ulkopinnat.
siihen eivät vaikuta kaikki hapot (vetyfluoridia lukuun ottamatta) ja kaikki emäkset.,
Hafnium reagoi halogeenien muodostaa tetrahalides, ja korkeissa lämpötiloissa se reagoi hiilen kanssa, boori, typpeä, happea, piitä ja rikkiä.
Käyttää Hafnium
Hafnium käytetään reaktorin säätösauvat, koska sen kyky absorboida neutroneja ja sen hyviä mekaanisia ja korroosionkesto-ominaisuuksia. Tämä on täydellinen vastakohta zirkoniumille, joka on kemiallisesti hyvin samanlainen kuin hafnium, on erittäin huono absorboimaan neutroneja., Zirkoniumia käytetään siis polttoainesauvojen verhouksessa (ulompi kerros), jonka läpi on tärkeää, että neutronit voivat kulkea helposti.
hafniumia käytetään myös valokuvaussalamalampuissa, hehkulampun filamenteissa sekä elektroniikkalaitteissa katodeina ja kondensaattoreina.
Hafniumseokset useiden muiden metallien, kuten raudan, niobiumin, tantaalin ja titaanin kanssa.
Hafnium-niobiumseokset ovat esimerkiksi lämmönkestäviä ja niitä käytetään ilmailu-ja avaruussovelluksissa, kuten avaruusrakettimoottoreissa.,
Hafnium carbide käytetään linja korkean lämpötilan uunit / uunit, koska sen tulenkestävät ominaisuuksia (se ei sula korkeissa lämpötiloissa).
Hafnium-pohjaisia yhdisteitä käytetään porttieristeissä tietokoneiden integroitujen piirien 45 nm: n sukupolvessa.
Hafnium oksidi-pohjainen yhdisteitä tuodaan pii-pohjainen pelimerkkejä tuottaa pienempiä, energiatehokkaampia ja suorituskyky pakattu prosessoria(4).
runsaus ja isotoopit
runsaus maankuori: 3,3 osaa miljoonassa painosta, 0.,4 miljoonasosaa myyrät
Runsaasti aurinkokunta: 1 part per billion paino, 0.01 ppm miljardia myyrät
Kustannukset, puhdas: $120 per 100g
Hinta, bulk: $ per 100g
Lähde: Hafnium ei löydy vapaasti luonnossa, mutta on useimmissa zirkonium mineraalien pitoisuus on välillä yksi ja viisi prosenttia. Kaupallisesti hafniumia valmistetaan zirkoniumin jalostuksen sivutuotteena. Tämä tapahtuu Kroll-prosessin avulla, jolloin tetrakloridi pelkistyy magnesiumin tai natriumin kanssa.,

- Kuva Deglr6328
- Per Enghag, Tietosanakirja Tekijät: Tekniset Tiedot – Historia – Käsittely – Sovelluksia, 2008, John Wiley & Pojat, p527.
- Bob Weintraub, George De Hevesy (1885 1966) (pdf-dokumentti).
- Aile Tamm, Atomikerrostuminen korkean Permittiivisyyden eristeistä Syklopentadienyylipohjaisista lähtöaineista, 2010, Tarton yliopiston lehdistö, p18.,
Cite this Page
online yhdistää, kopioi ja liitä jokin seuraavista:
<a href="https://www.chemicool.com/elements/hafnium.html">Hafnium</a>
tai
<a href="https://www.chemicool.com/elements/hafnium.html">Hafnium Element Facts</a>
mainita tämän sivun akateeminen asiakirja, käytä seuraavaa MLA-yhteensopiva viite:
"Hafnium." Chemicool Periodic Table. Chemicool.com. 17 Oct. 2012. Web. <https://www.chemicool.com/elements/hafnium.html>.