asetaali on funktionaalinen ryhmä, jonka liitettävyys on R2C(tai’)2). Täällä, R-ryhmät voivat olla orgaanisia fragmentteja (hiiliatomin, mielivaltaisia muiden atomien kiinnitetty siihen) tai vety, kun taas R-ryhmien tulee olla orgaaninen palasia ei vety. Kaksi R ’ – ryhmää voivat olla keskenään ekvivalentteja (”symmetrinen asetaali”) tai ei (”sekoitettu asetaali”)., Asetaalit muodostuvat ja vaihtovelkakirjalainan aldehydien tai ketonien ja on samalla hapetusasteella keski hiiltä, mutta on huomattavasti erilainen kemiallinen stabiilisuus ja reaktiivisuus verrattuna analoginen karbonyyli-yhdisteiden. Keskeisellä hiiliatomilla on siihen neljä sidosta, joten se on kylläinen ja sillä on tetraedrinen geometria.,

Yleinen rakenne asetaalit
termi valtioiden, alueiden käytetään joskus tunnistaa rakenteita, jotka liittyvät ketonit (sekä R-ryhmät orgaaniset palasia sijaan vety) sen sijaan, aldehydit ja historiallisesti termi acetal käytettiin erityisesti aldehydi-liittyvät tapaukset (ottaa ainakin yhden vedyn tilalle R keski-carbon). IUPAC alun perin vanhentunut sanan käyttö valtioiden, alueiden kokonaan, mutta on sittemmin perui päätöksensä., Vastakohtana historialliselle käytölle ketaalit ovat kuitenkin nykyisin asetaalien osajoukko, termi, joka käsittää nykyisin sekä aldehydi-että ketonijohdannaiset rakenteet.
Jos yksi R-ryhmät on happea kuin ensimmäinen atomi (että on olemassa enemmän kuin kaksi oxygens yhden liimata keski-carbon), toiminnallinen ryhmä on sen sijaan orthoester. R: n muunnelmista poiketen molemmat R ’ – ryhmät ovat orgaanisia fragmentteja. Jos yksi R’ on vety, toiminnallinen ryhmä on sen sijaan hemiacetal, kun taas jos molemmat ovat S, toiminnallinen ryhmä on ketoni hydraatti tai aldehydi kosteuttaa.,
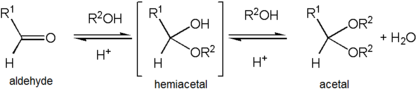
asetaalin muodostuminen tapahtuu, kun hemiasetaalin hydroksyyliryhmä protonoituu ja häviää vetenä. Tällöin syntyvän karbokationin kimppuun käy nopeasti alkoholimolekyyli. Protonin menetys kiinnittyneestä alkoholista antaa asetaalin.,
Acetals are stable compared to hemiacetals but their formation is a reversible equilibrium as with esters., Reaktiona luoda acetal etenee, vesi on poistettava reaktio seos, esimerkiksi, jossa Dean–Stark-laitteet, jottei se hydrolysoidaan tuotteen takaisin hemiacetal. Muodostumista asetaalit vähentää kokonaismäärä molekyylien läsnä (karbonyyli + 2 alkoholi → acetal + vesi), ja sen vuoksi ei yleensä ole suotuisa suhteen entropia. Yksi tilanne, jossa se ei ole entropically epäsuotuisat on, kun yksi dioli molekyyli käytetään sijasta kaksi erillistä alkoholin molekyylit (karbonyyli + glykoli → acetal + vesi)., Toinen tapa välttää entrooppiset kustannukset on tehdä synteesi, jonka acetal vaihto, käyttäen olemassa olevia acetal-reagenssin tyyppi kuin TAI’-ryhmä luovuttajan pikemminkin kuin yksinkertainen lisäksi alkoholit itse. Yksi menetelmässä käytetty reagenssityyppi on ortoesteri. Tässä tapauksessa, vesi tuotetaan yhdessä acetal tuote on tuhoutunut, kun se hydrolysoi jäljellä orthoester molekyylejä, ja tämä puoli reaktio tuottaa myös enemmän alkoholia käytetään pääasiassa reaktion.,
Asetaalit käytetään suojella ryhmiä karbonyyli-ryhmien orgaanisessa synteesissä, koska ne ovat stabiileja suhteessa hydrolyysin emäkset ja suhteessa monet hapettavat ja pelkistävät aineet. Ne voivat joko suojata karbonyyli molekyylin (tilapäisesti reagoi sen kanssa alkoholia) tai dioli (tilapäisesti reagoi sen kanssa karbonyyli). Eli joko karbonyyli, tai alkoholit, tai molemmat voisivat olla osa molekyylin, jonka reaktiivisuus on valvottava.
erilaisilla spesifisillä karbonyyliyhdisteillä on erityiset nimet asetaalimuodoilleen., Esimerkiksi acetal muodostuu formaldehydiä (kaksi vetyä liitetty keski-hiili) on joskus kutsutaan muodollinen tai methylenedioxy-ryhmä. Asetonista muodostuvaa asetaalia kutsutaan joskus asetonidiksi.