ilt er afgørende for livet. Alle vævsceller afhænger for deres funktion og overlevelse af den kontinuerlige generering af energi i form af adenosintrifosfat (ATP); denne ATP genereres i celler ved aerob metabolisme af diætbrændstoffer (hovedsageligt glukose) til kuldio .id og vand.
hvis tilførslen af ilt afbrydes, begrænses eller ophører denne energifrembringende proces med resulterende celleskade og i sidste ende celledød og organsvigt .,
Utilstrækkelige ilt i væv, kaldet iltsvind, er den mest almindelige årsag til celle personskade/død og som er afgørende for, eller i det mindste en medvirkende faktor i, etiology og/eller patogenesen af de mest potentielt livstruende sygdomme/forhold, set i akutte og critical care medicine .
for at forstå, hvordan arteriel blodgasresultater hjælper med at vurdere patientens risiko for vævshypo .i, er en grundlæggende viden om ilttransport i blod nødvendig.,
ilttransport i blod
en primær funktion af åndedræts-og kardiovaskulære systemer er levering af inspireret (atmosfærisk) ilt til vævsceller. Denne leveringsproces begynder ved lungernes alveolære kapillære membran.
inspireret ilt til stede i alveolære luftdiffuses fra alveoler – de mikroskopiske blindsække af lungestruktur-til blod, der strømmer gennem lungekapillærerne, der omgiver hver alveolus.,
blod, der nu er fyldt med ilt, overføres fra lungerne via arteriesystemet til vævets mikrovaskulatur, hvor ilt frigives til vævsceller.
iltfattige blod er viderebragt fra væv microvasculature via det venøse system tilbage til højre side af hjertet, og videre via den pulmonale arterie til lungerne, for fornyet iltning.
ilt er dårligt opløseligt i blod, og den lille maksimale mængde ilt, der kan transporteres simpelthen opløst i blod, er ret utilstrækkelig til at tilfredsstille kroppens efterspørgsel efter ilt.,
faktisk opløses kun 1-2% af det ilt, der transporteres i blod, i blodet; det er denne lille fraktion, der afspejles i det målte partialtryk af ilt i arterielt blod (pO2(a)).
de resterende 98-99% transporteres i erytrocytter bundet reversibelt til protein hæmoglobin.
iltleveringsfunktionen af hæmoglobin, dvs., dens evne til at “afhente” ilt i lungerne og” frigive ” det i vævets mikrovaskulatur muliggøres ved en reversibel ændring i strukturen af hæmoglobinmolekylet, der ændrer dets affinitet for ilt, og dermed mængden af ilt hvert molekyle bærer .
en række miljøfaktorer i blod bestemmer hæmoglobinets relative affinitet for ilt.
den mest betydningsfulde af disse er pO2. Hæmoglobin til stede i blod med relativt høj pO2 har meget større affinitet for ilt end hæmoglobin til stede i blod med relativt lav pO2., O oxygenygendissociationskurven (ODC) beskriver dette forhold grafisk (se fig. 1).
procentdelen af total hæmoglobin, der er mættet med ilt (dvs.iltmætning, sO2) er målet for hæmoglobinaffinitet i denne graf.
Det er tydeligt på grafen, at ved de høje pO2, der hersker i blodet udsat for alveolære luft i lungerne (~12 kPa), hæmoglobin er næsten 100 % mættet med ilt; næsten alle ilt-binding sites på helheden af hæmoglobin-molekyler, der er optaget med ilt.,
i modsætning hertil i vævets miljø, hvor pO2 er meget lavere, er hæmoglobinaffinitet for ilt også meget lavere, og ilt frigives fra hæmoglobin til vævene.
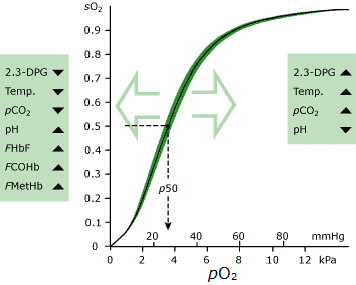
Fig1: OCD
Selv om pO2(a) kun afspejler en meget lille andel (1-2 %) af ilt i arterielt blod, det er meget vigtig, fordi, som ODC indebærer, det bestemmer mængden af ilt bundet til hæmoglobin i arterielt blod (sO2(a)) og derfor er den samlede mængde af ilt, der er indeholdt i arterielt blod til levering til væv.,
Hvis pO2(a) reduceres, kan mindre ilt bæres af hæmoglobin (dvs.sO2(a) reduceres), og mindre ilt er tilgængeligt for væv. Undersøgelse af ODC viser, at et signifikant fald i pO2(a) fra 15 til 10 kPa kPa har kun lille effekt på sO2(a), og derfor ilt indhold af arterielt blod, men der er et markant fald i sO2(a), som pO2(a) falder under ca 9-10 kPa.
tilførslen af ilt til væv bliver i stigende grad kompromitteret, da pO2(a) falder under dette niveau.,
For tilstrækkelig iltning af væv:
- blod skal indeholde normal koncentration af hæmoglobin
- at hæmoglobin skal være >95 % mættet med ilt i arterielt blod (sO2(a) >95 %)
- for at opnå sO2(a) >95 %, pO2(a) skal være >10 kPa (se ODC)
- vedligeholdelse af normal pO2(a), eller i det mindste pO2(a) på over 10 kPa, er afhængige af en passende sats af ilt ved diffusion fra alveolerne til pulmonal kapillær blod, dvs, normale alveolære ventilation og perfusion
DEFINITION AF ARTERIEL ILT SATURATION (sO2(a))
iltmætning afspejler kun ilt i blodet, der er bundet til hæmoglobin, ikke det lille beløb, der er opløst i blod plasma.
hæmoglobinmolekylet siges at være “mættet” med ilt, når alle dets fire iltbindende steder er optaget af ilt; produktet af denne binding kaldes o .yhemoglobin.
iltmætning er procentdelen af totale hæmoglobinbindingssteder, der er tilgængelige til binding til ilt, der er optaget af ilt.,
Det er således et mål for, hvor meget af det iltbærende kapacitet på grund af hæmoglobin bliver udnyttet, og er defineret ved følgende ligning:
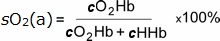 Eqtn 1
Eqtn 1
hvor cO2Hb = koncentration af oxyhemoglobin i arterielt blod
cHHb = koncentration af deoxyhemoglobin i arterielt blod
(cO2Hb + cHHb = koncentrationen af total hæmoglobin i stand til bindende
oxygen)
Det er vigtigt at bemærke, at nævneren i denne ligning er ikke koncentrationen af total hæmoglobin.,
Der er to arter af hæmoglobin til stede i blod, der ikke er i stand til at binde ilt og derfor ikke er inkluderet i nævneren. De er Carbo .yhemoglobin (COHb) og methemoglobin (MetHb), sammen kaldet dyshemoglobinerne på grund af deres funktionelle redundans.
I sundhed, COHb og MetHb tilsammen udgør mindre end ~5 % af de samlede hæmoglobin, så normalt, at koncentrationen af total hæmoglobin (ctHb) beregner summen af cO2Hb og cHHb.,
Der er dog patologier – især kulilteforgiftning og methemoglobinæmi – der er forbundet med en markant stigning i COHb eller MetHb og en resulterende markant reduktion i blodets iltbærende kapacitet, som ikke afspejles i sO2(a).
tilsvarende reducerer reduktion i ctHb (dvs.anæmi) også blodets iltbærende kapacitet, men fremkalder ingen ændring i sO2(a). Reduktion i sO2 (a) opstår kun som et resultat af tilstande(lunge og ikke-lunge), der forårsager reduktion i pO2 (a).,
sO2 (A) (eller SpO2) inden for det (normale) referenceområde (95-98%) er således ingen garanti for, at blodet er godt iltet, langt mindre at vævene er tilstrækkeligt iltet.
MÅLING AF sO2(a) VED CO-OXIMETRY
Mange moderne blod gas analysatorer har en indbygget CO-oximeter, der giver direkte måling af sO2(en). Denne måling er baseret på spektrofotometrisk analyse af hæmoglobinet frigivet fra en prøve af hæmolyseret arterielt blod .,
De fire hæmoglobin arter, der findes i blodet (oxyhemoglobin, O2Hb; deoxyhemoglobin, HHb; carboxyhemoglobin, COHb, og methemoglobin, MetHb), som hver har en karakteristisk lys-absorptionsspektrum.
måling af mængden af lys absorberet af den hæmolyserede prøve ved flere specifikke bølgelængder muliggør nøjagtig bestemmelse af koncentrationen af hver af de fire hæmoglobinarter. Koncentrationen af O2Hb og HHb gør det muligt at udlede sO2(a) (se ligning 1 ovenfor).,
Denne metode af sO2(a) målingen giver samtidig produktion af yderligere parametre:
- samlet hæmoglobin, ctHb (cO2Hb + cHHb + cCOHb + cMetHb)
- fraktioneret carboxyhemoglobin, FCOHb (cCOHb / ctHb × 100)
- fraktioneret methemoglobin, FMetHb (cMetHb / ctHb × 100)
- fraktioneret oxyhemoglobin FO2Hb (cO2Hb / ctHb × 100)
BEREGNING AF sO2(en)
Forud for udvikling af blod gas analysatorer med indbygget CO-oximeters,sO2(a) kunne kun blive genereret i løbet af blod gas analyse ved beregning ud fra målt pO2(en).,
nogle blodgasanalysatorer, der er i brug i dag, har ikke et inkorporeret CO-o .imeter, så generering af beregnede sO2(a) værdier under blodgasanalyse fortsætter.
Beregning af sO2(a) målt pO2(a) er baseret på forholdet mellem de to, som er beskrevet af ilt dissociation kurve (ODC); beregning er en matematisk beskrivelse af kurven.
heri ligger den potentielle mangel på beregnet sO2(a), fordi formen og placeringen af ODC påvirkes af andre faktorer end pO2(A) og sO2(a)., Den vigtigste af disse er:
- temperatur
- pH
- pCO2
- koncentrationen af 2,3-diphosphoglycerate (2,3-DPG)
- koncentrationen af dyshemoglobins (carboxyhemoglobin, methemoglobin)
standard (normal) ODC vedrører pO2(a) og sO2(a) i blod ved standard betingelser (pH 7.4, pCO2 40 mmHg, og temperatur på 37 °C). Denne standardkurve antager også normale koncentrationer af 2,3-DPG og dyshemoglobin (COHb og MetHb).,
kurven forskydes til højre (som betyder lavere sO2(a) for en given pO2(a)) ved nogen af følgende:
- Øget temperatur >37 °C
- Øget pCO2 >40 mmHg, 5.3 kPa
- Nedsat pH
- Øget 2,3-DPG
kurven forskydes til venstre (hvilket betyder højere sO2(a) for en given pO2(a)) ved nogen af følgende:
- Nedsat temperatur
- Nedsat pCO2
- Øget pH >7.,4
- Øget koncentration af dyshemoglobin (COHb eller MetHb)
- Faldt 2,3-DPG
Til bedre at forstå, hvordan disse variabler påvirker ODC, er det nyttigt at få vist en virtuel interaktive ilt dissociation kurve; den ene er til rådighed på: www.ventworld.com/resources/oxydisso/dissoc.html
For den generation af beregnet sO2(a), blod gas analysatorer anvende en af en række af komplekse algoritmer, der er blevet udviklet til beregning af sO2(a) målt pO2(en) .,
på en eller anden måde forsøger de alle at tage hensyn til nogle af de ovenfor beskrevne variabler, der påvirker ODC. Disse algoritmer kræver input ikke kun målt pO2(a), men også målt pH og i nogle tilfælde målt pCO2(a) eller beregnede base excess.
alle antager normal 2,3-DPG, og nogle antager ingen unormal stigning i dyshæmoglobinerne, COHb og MetHb.,
Mens disse algoritmer give tilstrækkeligt præcist estimat af sO2(a) for raske personer, og de fleste patientgrupper uden hypoxemia, er dette ikke nødvendigvis tilfældet for hypoxemic kritisk syg patient, som måske derudover har: svær syre-base-forstyrrelse; blive underafkølet eller hyperthermic; unormal 2,3-DPG eller markant stigning i dyshemoglobins .,
med andre ord, i betragtning af antallet af faktorer, der påvirker ODC samt det komplekse samspil mellem disse faktorer, er det simpelthen ikke muligt med et enkelt matematisk sammenhæng, uanset hvor sofistikeret, til at beskrive tilstrækkeligt præcist den præcise form og position af den ilt, dissociation kurve for alle blodprøver fra kritisk syge patienter.,
potentielle unøjagtigheder i forbindelse med beregning af sO2(a) fra et enkelt matematisk interpolation af ilt dissociation kurven er godt påvist ved resultater af en undersøgelse, som analyse af 10,079 arterielle blod gas resultater, der alle stammer fra patienter, hvis kliniske tilstand krævede blod gas analyse (dvs akut kritisk syge individer).,
Siden beregnet sO2(a) er baseret på interpolation af ODC, fejl er uundgåeligt større for hypoxemic arterielle prøver og alle venøse prøver, fordi disse er at undersøge den stejle del af kurven, hvor ganske små fejl i pO2 målinger har markant effekt på sO2.,
BEREGNET (SKØNNET) sO2(a) OG sO2(v) BØR IKKE BRUGES til AT BEREGNE ANDRE VARIABLER AF ILT TRANSPORT, LEVERING OG FORBRUG
iltmætning værdier i arteriel bloodsO2(a) og blandet veneblod (sO2(v)) er brugt i beregninger til at bestemme andre klinisk nyttige parametre for vurdering af hypoxi risiko blandt de kritisk syge .,
hovedårsagen til at foretrække direkte målt iltmætning frem for beregnet (estimeret) iltmætning er baseret på forestillingen om, at den iboende potentielle fejl ved beregning af iltmætning skitseret ovenfor forstærkes under beregning af disse yderligere parametre.
for at forstå, hvordan denne fejlforstærkning kan forekomme, er det vigtigt først at definere nogle af disse afledte parametre: ctO2(a), DO2 og VO2.
fuld vurdering af iltlevering til væv kræver viden om det totale iltindhold i arterielt blod, ctO2(a)., Dette er summen af den ilt, der er opløst i blod og ilt bundet til hæmoglobin og er beregnet under arterielt blod gas analyse ved hjælp af følgende ligning:
ctO2(a) (ml/L) = (k1 × ctHb x sO2(a)) + (k2 × pO2(a)) Eqtn 2
hvor ctHb = koncentrationen af total hæmoglobin (g/L)
sO2(a)= ilt mætning af arterielt blod (%)
pO2(a) = partialtrykket af ilt i arterielt blod (kPa)
k1 er en konstant (ilt-bindende kapacitet af hæmoglobin) = 1.31 mL/g
k2 er en konstant (opløselighed fordelingskoefficient af ilt ved 37 °C) = 0.,23
mL/L/kPa)
ctO2(a), til gengæld giver mulighed for beregning af globale ilt (DO2), dvs. mængden af ilt, der leveres fra lungerne til væv hvert minut . Dette afhænger af to parametre: koncentration af ilt i arterielt blod og total blodgennemstrømning i enhedstid (dvs ., cardiac output, CO) og er udtrykt ved følgende ligning:
DO2 (mL/min) = ctO2(a) × CO Eqtn 3
hvor CO = minutvolumen i mL/min (normalt omkring 5 L/min)
Dette forhold understreger, at væv hypoxi kan (og gør det ofte) sker på trods af normale blodets iltning. Tilstrækkelig tilførsel af ilt til væv trues ikke kun af utilstrækkelig iltning af blodet, men også af reduceret blodgennemstrømning.
kendskab til ctO2 (a) tillader også beregning af globalt iltforbrug (VO2), dvs., mængden af ilt forbruges af væv i enhedstid . Denne beregning kræver også kendskab til ctO2 (v), koncentrationen af ilt i blandet venøst blod.
dette genereres under blodgasanalyse af blod udtaget via et lungearteriekateter (dvs .blandet venøst blod). Det beregnes ud fra målt partialtryk(pO2 (v)), iltmætning(sO2 (V)) og hæmoglobinkoncentration (ctHb) som i ligning 2 (ovenfor) for arterielt blod.,
Den ligning til beregning af VO2 er:
VO2 (mL/min) = CO x Eqtn 4
risikoen for væv hypoxi er øget, hvis væv er tidskrævende supranormal mængder af ilt (dvs VO2 er øget), som godt kan være tilfældet for nogle patienter, der lider af kritisk sygdom .
det er klart, at nøjagtigheden af alle disse afledte parametre i vid udstrækning afhænger af nøjagtigheden af iltmætningsværdier (sO2(A) og sO2(v)).,
En række undersøgelser har påvist en klinisk signifikant forskel, hvis beregnede værdier for sO2(a)/sO2(v), snarere end CO-oximeter-genereret målte værdier, bruges til at bestemme disse afledte parametre.
forfatterne til alle disse undersøgelser konkluderer, at for klinisk pålideligt skøn over de afledte variable, såsom VO2 og DO2, sO2(a) og sO2(v) skal måles direkte ved CO-oximetry; beregnede værdier er ikke egnede.
det samme råd er indeholdt i retningslinjer fra Clinical and Laboratory Standards Institute .,
OVERSIGT
- iltmætning (sO2) er en parameter, der anvendes i klinisk medicin til at vurdere, blodets iltning af blodet og dermed risikoen for væv hypoxi.
- iltmætning overvåges oftest ikke-invasivt ved pulso .imetri, men denne tilgang har begrænsninger.
- en fyldigere og mere præcis vurdering af blodo .ygenering tilbydes ved arteriel blodgasanalyse. O .ygenmætning er kun en af flere O .ygenrelaterede parametre, der genereres under blodgasanalyse.,
- iltmætning genereres under blodgasanalyse ved en af to metoder: direkte måling ved CO-o .imetri; eller beregnet ud fra målt pO2.
- beregningen, der bruges til at generere sO2 fra pO2(A), er baseret på forholdet mellem de to beskrevet af O .ygendissociationskurven.
- ilt dissociation kurven er påvirket af en række andre faktorer end pO2 og sO2, der kan være i en tilstand af stor flux under kritisk sygdom, der gør beregnet sO2 potentielt forkerte.,
- Måles sO2 (ved CO-oximetry) er upåvirket af disse strømme; det er den foretrukne metode til bestemmelse af ilt mætning og mest almindeligt anvendte i dag (mest moderne blod gas analysatorer har en indbygget CO-oximeter)
- Behandlere bør være opmærksomme på den metode, der anvendes til at generere sO2 i løbet af blod gas analyse på deres institution. Hvis metoden beregnes ud fra målt pO2, skal sO2-værdier fra kritisk syge patienter fortolkes med forsigtighed., Uoverensstemmelse mellem pO2(a) og beregnet sO2 (for eksempel, en angivelse af hypoxemia og andre, der angiver normoxemia) tyder på, at en forkert beregnet sO2(a) værdi.
- beregnede sO2-værdier bør ikke bruges til at beregne yderligere O .ygenrelaterede variabler som DO2 og VO2; kun direkte målte sO2-værdier bør anvendes i disse beregninger.