en acetal er en funktionel gruppe med forbindelsen R2C(eller’)2). Her kan R-grupperne være organiske fragmenter (et carbonatom, med vilkårlige andre atomer bundet til det) eller hydrogen, mens R’ – grupperne skal være organiske fragmenter ikke hydrogen. De to R ‘ grupper kan svare til hinanden (en “symmetrisk acetal”) eller ej (en “blandet acetal”)., Acetaler dannes af og konverteres til aldehyder eller ketoner og har den samme o .idationstilstand ved det centrale kulstof, men har væsentligt forskellig kemisk stabilitet og reaktivitet sammenlignet med de analoge carbonylforbindelser. Det centrale carbonatom har fire bindinger til det, og er derfor mættet og har tetrahedral geometri.,

Generisk struktur af acetaler
udtrykket ketal er undertiden bruges til at identificere de strukturer, der er forbundet med ketoner (både F grupper organiske fragmenter snarere end brint) snarere end aldehyder og historisk, udtrykket acetal var der anvendes specifikt for aldehyd-relaterede sager (der mindst én brint i stedet for et R på den centrale kulstof). IUPAC afskrev oprindeligt brugen af ordet ketal helt, men har siden vendt sin beslutning., Imidlertid, i modsætning til historisk brug, ketaler er nu en undergruppe af acetaler, et udtryk, der nu omfatter både aldehyd – og ketonafledte strukturer.
Hvis en af R grupper har en ilt som det første atom (det er, der er mere end to oxygens enkelt-bundet til den centrale kulstof), den funktionelle gruppe er i stedet en orthoester. I modsætning til variationer af R er begge R ‘ grupper organiske fragmenter. Hvis en R ‘ er et brint, er den funktionelle gruppe i stedet en hemiacetal, mens hvis begge er H, er den funktionelle gruppe et ketonhydrat eller aldehydhydrat.,
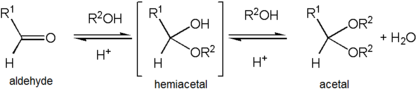
dannelse af et acetal forekommer, når hydro .ylgruppen af en hemiacetal bliver protoneret og går tabt som vand. Den carbocation, der produceres, angribes derefter hurtigt af et alkoholmolekyle. Tab af protonen fra den vedhæftede alkohol giver acetalen.,
Acetals are stable compared to hemiacetals but their formation is a reversible equilibrium as with esters., Som en reaktion på at skabe et acetalprovenu skal vand fjernes fra reaktionsblandingen, for eksempel med et Dean–Stark-apparat, for at det ikke hydrolyserer produktet tilbage til hemiacetalet. Dannelsen af acetaler reducerer det totale antal tilstedeværende molekyler (carbonyl + 2 alkohol + acetal + vand) og er derfor generelt ikke gunstig med hensyn til entropi. En situation, hvor det ikke er entropisk ugunstigt, er, når der anvendes et enkelt diolmolekyle snarere end to separate alkoholmolekyler (carbonyl + diol + acetal + vand)., En anden måde at undgå de entropiske omkostninger er at udføre syntesen ved acetal udveksling, ved hjælp af en allerede eksisterende acetal-type reagens som eller’-gruppe donor snarere end simpel tilsætning af alkoholer selv. En type reagens, der anvendes til denne metode, er en orthoester. I dette tilfælde ødelægges vand produceret sammen med acetalproduktet, når det hydrolyserer resterende orthoestermolekyler, og denne sidereaktion producerer også mere alkohol, der skal anvendes i hovedreaktionen.,acetaler anvendes som beskyttelsesgrupper for carbonylgrupper i organisk syntese, fordi de er stabile med hensyn til hydrolyse af baser og med hensyn til mange o .iderende og reducerende midler. De kan enten beskytte carbonylen i et molekyle (ved midlertidigt at reagere det med en alkohol) eller en diol (ved midlertidigt at reagere det med en carbonyl). Det vil sige enten carbonylen eller alkoholerne eller begge dele kunne være en del af molekylet, hvis reaktivitet skal kontrolleres.forskellige specifikke carbonylforbindelser har særlige navne for deres acetalformer., For eksempel kaldes et acetal dannet af formaldehyd (to hydrogener bundet til det centrale kulstof) undertiden en formel eller methylendio .ygruppen. Acetalet dannet af acetone kaldes undertiden et acetonid.