acetal je funkční skupina s konektivitou R2C(nebo‘)2). Zde, R skupiny mohou být organické fragmenty (atom uhlíku, s libovolnými jinými atomy připojené k), nebo vodík, zatímco R‘ skupiny musí být organické fragmenty ne vodík. Obě skupiny R ‚ mohou být navzájem rovnocenné („symetrický acetal“) nebo ne („smíšený acetal“)., Acetaly jsou tvořeny z a převést na aldehydy nebo ketony a mají stejné oxidační stav na centrálním uhlíku, ale mají podstatně odlišné chemické stabilitě a reaktivitě ve srovnání s obdobným karbonylové sloučeniny. Centrální atom uhlíku má k němu čtyři vazby, a proto je nasycený a má čtyřstěnnou geometrii.,

Obecné struktury acetaly
termín ketal je někdy používán k identifikaci struktury spojené s ketony (oba R. skupin organických fragmentů, spíše než vodík), spíše než aldehydy a, historicky, termín acetalový byl použit speciálně pro aldehyd-související případech (které mají alespoň jeden vodík na místo R na centrální uhlík). IUPAC původně zastaralé použití slova ketal úplně, ale od té doby obrátil své rozhodnutí., Nicméně, na rozdíl od historického použití, ketály jsou nyní podmnožinou acetalů, termín, který nyní zahrnuje jak aldehydové, tak ketonové struktury.
Pokud jeden z R skupin má kyslík jako první atom (to je, tam jsou více než dva kyslíky single-vázané na centrální uhlík), funkční skupina je místo orthoester. Na rozdíl od variací R jsou obě skupiny R organické fragmenty. Pokud jeden R je vodík, funkční skupiny je místo hemiacetal, zatímco pokud jsou oba H, funkční skupiny je keton hydrát nebo aldehyd hydrataci.,
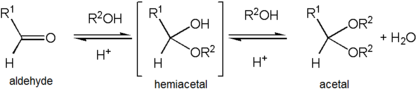
tvorba acetalu nastává, když se hydroxylová skupina hemiacetalu protonuje a ztrácí se jako voda. Karbokace, která se vyrábí, je pak rychle napadena molekulou alkoholu. Ztráta protonu z připojeného alkoholu dává acetal.,
Acetals are stable compared to hemiacetals but their formation is a reversible equilibrium as with esters., Jako reakce na vytvoření acetalový výnosů, voda musí být odstraněny z reakční směsi, například s Dean–Stark přístroje, jinak to hydrolyzovat produktu zpět na hemiacetal. Tvorba acetalů snižuje celkový počet přítomných molekul (karbonyl + 2 alkohol → acetal + voda), a proto není obecně příznivá pro entropii. Jednou z situací, kdy není entropicky nepříznivá, je použití jediné molekuly diolu spíše než dvou samostatných molekul alkoholu (karbonyl + diol → acetal + voda)., Další způsob, jak se vyhnout entropické cena je provést syntézu acetalový exchange, pomocí pre-existující acetalový-typ činidla jako NEBO-skupina dárců, spíše než jednoduché přidání alkoholy sami. Jedním typem činidla použitého pro tuto metodu je ortoester. V tomto případě, vody vyrobené spolu s acetalový produkt je zničen, když to hydrolyzuje zbytkové orthoester molekuly, a na této straně reakce produkuje také více alkoholu, aby být použity v hlavní reakce.,
Acetaly jsou používány jako ochrana skupiny pro karbonylových skupin v organické syntéze, protože jsou stabilní vůči hydrolýze základny a s ohledem na mnoho oxidační a redukční činidla. Mohou buď chránit karbonyl v molekule (dočasnou reakcí s alkoholem) nebo diol (dočasnou reakcí s karbonylem). To znamená, že buď karbonyl, nebo alkoholy, nebo oba mohou být součástí molekuly, jejíž reaktivita má být kontrolována.
různé specifické karbonylové sloučeniny mají zvláštní názvy pro jejich acetalové formy., Například acetal vytvořený z formaldehydu (dva hydrogeny připojené k centrálnímu uhlíku) se někdy nazývá formální nebo methylendioxy skupina. Acetal vytvořený z acetonu se někdy nazývá acetonid.